题目内容
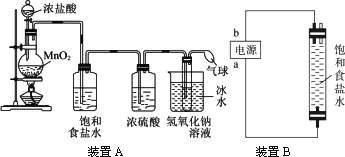
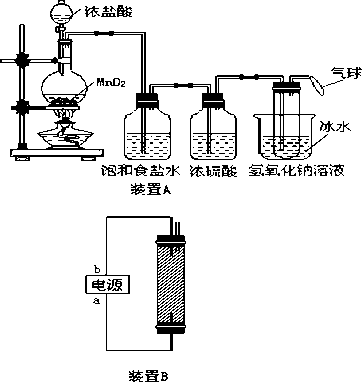
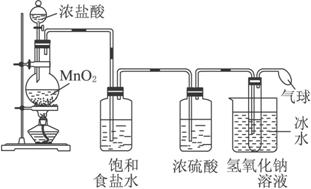
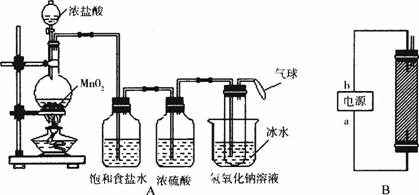
某研究小组为制备消毒液(主要成分NaClO)设计了A、B两套装置,如下图所示,并查阅到下列资料:在加热情况下卤素和碱液能发生如下反应:3X2+6OH-![]() 5X-+
5X-+![]() +3H2O
+3H2O

完成下列问题:
(1)装置A的大试管内发生反应的离子方程式为___________________________。
(2)装置中A能否省去冰水冷却?_________,理由是_________________________________。
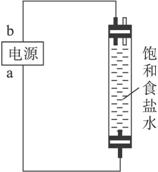
(3)写出装置B电解的化学反应方程式____________________________________。
(4)b极是电源的_________极,理由是____________________________________。
(1)Cl2+2OH-![]() Cl-+ClO-+H2O
Cl-+ClO-+H2O
(2)不能 因为Cl2与碱液的反应放热,会使溶液温度升高而发生副反应。
(3)2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(4)正 电解池阳极在下端,生成的Cl2向上扩散,与NaOH溶液充分接触反应,上端为阴极,便于产生的H2逸出
解析:本题在信息的条件下设计实验,考查学生的对比分析能力。A为Cl2的实验室制法,试管中用氢氧化钠溶液吸收Cl2,用冰水冷却降温,否则会发生副反应。装置B为电解饱和的NaCl溶液,生成的Cl2向上扩散,与NaOH溶液充分接触反应,所以下端为电解池阳极,所以b极是电源的正极。

 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
| |||||||||||||||||||||||||||||||||