题目内容
 五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:(1)A原子核外电子总数是内层电子数的三倍,A、E同主族
(2)B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H.
(3)C的焰色应呈黄色.
(4)D在同周期主族元素形成的简单离子中,离子半径最小.
回答下列问题:
(1)写出D在元素周期表中的位置:
(2)化合物H的水溶液PH
(3)上述元素的最高价氧化物对应的水化物中,有一种物质在一定条件下均能与其他四种物质发生化学反应,写出该物质的电子式
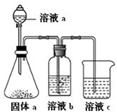
(4)某同学设计实验证明A、B、E的非金属性强弱关系.
①溶液a和b分别为
考点:位置结构性质的相互关系应用,非金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:五种短周期元素A、B、C、D、E原子序数依次增大,(1)A原子核外电子总数是内层电子数的三倍,则A为碳元素,A、E同主族,则E为硅元素,(2)B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H,则B为氮元素,F为硝酸,G为氨气,H为硝酸铵,(3)C的焰色应呈黄色,则C为钠元素,(4)D在同周期主族元素形成的简单离子中,离子半径最小,且原子序数等于钠,则D为铝元素,据此答题;
解答:
解:五种短周期元素A、B、C、D、E原子序数依次增大,(1)A原子核外电子总数是内层电子数的三倍,则A为碳元素,A、E同主族,则E为硅元素,(2)B的最高价氧化物对应的水化物F与其气态氢化物G反应,得到离子化合物H,则B为氮元素,F为硝酸,G为氨气,H为硝酸铵,(3)C的焰色应呈黄色,则C为钠元素,(4)D在同周期主族元素形成的简单离子中,离子半径最小,且原子序数大于钠,则D为铝元素,
(1)D为铝元素,在元素周期表中处于第三周期第ⅢA族,
故答案为:第三周期第ⅢA族;
(2)化合物H为硝酸铵,由于铵根离子水解,它的水溶液呈酸性,所以PH<7,离子方程式为NH4++H2O?NH3.H2O+H+,
故答案为:NH4++H2O?NH3.H2O+H+;
(3)上述元素的最高价氧化物对应的水化物中,氢氧化钠在一定条件下均能与其他四种物质发生化学反应,它的电子式为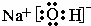 ,
,
故答案为: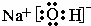 ;
;
(4)元素的非金属性越强,对应的最高价含氧酸的酸性越强,根据强酸制弱酸的原理设计实验,溶液a和b分别为硝酸、饱和碳酸氢钠溶液,溶液c中的离子方程式为CO2+SiO32-+H2O=H2SiO3↓+CO32-,或2CO2+SiO32-+2H2O=H2SiO3↓+2HCO3-,
故答案为:硝酸;饱和碳酸氢钠溶液;CO2+SiO32-+H2O=H2SiO3↓+CO32-,或2CO2+SiO32-+2H2O=H2SiO3↓+2HCO3-;
(1)D为铝元素,在元素周期表中处于第三周期第ⅢA族,
故答案为:第三周期第ⅢA族;
(2)化合物H为硝酸铵,由于铵根离子水解,它的水溶液呈酸性,所以PH<7,离子方程式为NH4++H2O?NH3.H2O+H+,
故答案为:NH4++H2O?NH3.H2O+H+;
(3)上述元素的最高价氧化物对应的水化物中,氢氧化钠在一定条件下均能与其他四种物质发生化学反应,它的电子式为
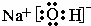 ,
,故答案为:
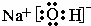 ;
;(4)元素的非金属性越强,对应的最高价含氧酸的酸性越强,根据强酸制弱酸的原理设计实验,溶液a和b分别为硝酸、饱和碳酸氢钠溶液,溶液c中的离子方程式为CO2+SiO32-+H2O=H2SiO3↓+CO32-,或2CO2+SiO32-+2H2O=H2SiO3↓+2HCO3-,
故答案为:硝酸;饱和碳酸氢钠溶液;CO2+SiO32-+H2O=H2SiO3↓+CO32-,或2CO2+SiO32-+2H2O=H2SiO3↓+2HCO3-;
点评:本题主要考查了元素周期表、盐类的水解、电子式、实验方案设计等知识,有一定的综合性,中等难度,解题时要注意元素化合物知识的灵活运用.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温常压下,22.4 L乙烯中C-H键数为4 NA |
| B、1 mol羟基中电子数为10 NA |
| C、在反应KIO3+6HI═KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA |
| D、常温下,1 L 0.1 mol/L NH4NO3溶液中NH4+的数目小于6.02×1022 |
现在在公路上经常能看到一些油罐车,这些车上应该贴的图标是( )
A、 |
B、 |
C、 |
D、 |
由碘乙烷制取乙二醇,依次发生反应的类型是( )
| A、取代 加成 水解 |
| B、消去 加成 取代 |
| C、水解 消去 加成 |
| D、消去 水解 取代 |
下列实验设计及其对应的离子方程式均正确的是( )
| A、氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
| B、Na2O2与H2O反应制备O2:Na2O2+H2O═2Na++2OH-+O2↑ |
| C、将氯气溶于水制备次氯酸:Cl2+H2O═2H++Cl-+ClO- |
| D、向Ba(OH)2溶液中滴加H2SO4溶液:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O |
若A+酸→盐+水,则A不可能属于( )
| A、氧化物 | B、单质 | C、碱 | D、电解质 |