题目内容
用氢氧化钠的标准溶液滴定未知浓度的稀盐酸,如果在配制氢氧化钠的标准溶液时混有Na2CO3,则测量的盐酸浓度会 .
考点:化学方程式的有关计算
专题:
分析:根据发生的反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,NaOH+HCl=NaCl+H2O,可知相同质量的碳酸钠、NaOH中,NaOH消耗HCl的物质的量更多,配制标准溶液的氢氧化钠中混有Na2CO3杂质,相当于标准的氢氧化钠的浓度偏小,据此判断.
解答:
解:由于氢氧化钠的性对分子量为40,而碳酸钠的性对分子量为100,根据发生的反应:Na2CO3+2HCl=2NaCl+CO2↑+H2O,NaOH+HCl=NaCl+H2O,可知相同质量的碳酸钠、NaOH,NaOH消耗HCl的物质的量更多,故配制标准溶液的氢氧化钠中混有Na2CO3杂质,相当于标准的氢氧化钠的浓度偏小,消耗氢氧化钠溶液的体积判断,测定盐酸的浓度偏高,故答案为:偏高.
点评:本题考查酸碱滴定误差分析,酸碱滴定是历年高考考查的重点,考查侧重考查学生的分析能力,关键是明确滴定原理,该题难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
由Fe2O3、Fe、CuO、C、Al中的几种物质组成的混合粉末,取样品进行下列实验(部分产物略去).关于混合粉末的组成判断正确的是( )
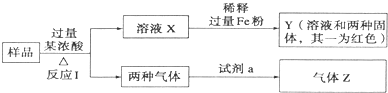

| A、一定含CuO和C |
| B、一定含Fe2O3、CuO和C |
| C、一定含CuO和C,一定不含Al |
| D、不管试剂a为H2O或饱和NaHCO3溶液,气体Z都为纯净物 |
甲酸是一种有机酸,又叫蚁酸.蚊子、蜂、蚂蚁等昆虫叮咬人时,会向人体射入蚁酸,使皮肤红肿、瘙痒,甚至疼痛.要消除这种症状,可在叮咬处涂抹下列物质中的( )
已知家庭中一些常见物质的pH:食醋-4;牙膏-9;食盐水-7;肥皂水-10;火碱液-13.
已知家庭中一些常见物质的pH:食醋-4;牙膏-9;食盐水-7;肥皂水-10;火碱液-13.
| A、火碱液 | B、食盐水 |
| C、牙膏或肥皂水 | D、食醋 |
下列溶液与100mL0.5mol/LNa2SO4溶液中的 Na+的物质的量浓度相等的是( )
| A、200mL0.5mol/LNaCl溶液 |
| B、100mL1mol/LNa2CO3溶液 |
| C、100mL0.5mol/LNa3PO4溶液 |
| D、1L1mol/LNaOH溶液 |
下列说法正确的是( )
| A、共价键都是极性的 |
| B、共价键的键能越大,共价键越牢固,含有该键的双原子分子越稳定 |
| C、CF4、CCl4、CBr4、CI4中C-X键的键长、键角均相等 |
| D、H2O分子中2个O-H键夹角为180° |
下列离子方程式中,正确的是( )
| A、稀硫酸滴在铜片上:Cu+2H+═Cu2++H2↑ |
| B、氧化镁与稀盐酸混合:MgO+2H+═Mg2++H2O |
| C、碳酸钡与盐酸:CO32-+2H+═H2O+CO2↑ |
| D、Ba(OH)2加入H2SO4:Ba2++SO42-═BaSO4↓ |
 五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息:
五种短周期元素A、B、C、D、E原子序数依次增大,结合下列信息: