题目内容
某3g醛和足量的银氨溶液反应,结果析出43.2g Ag,则该醛为( )
| A、甲醛 | B、乙醛 | C、丙醛 | D、丁醛 |
考点:有机物的推断,醛类简介
专题:有机物的化学性质及推断
分析:一元醛中甲醛与Ag的物质的量之比为1:4,其它一元醛与生成Ag的物质的量之比为1:2,若不是甲醛,求出醛的物质的量,然后计算其摩尔质量判断,若为甲醛,计算生成Ag的物质的量进行验证.
解答:
解:43.2g Ag的物质的量=
=0.4mol,
若不是甲醛,则醛的物质的量为
=0.2mol,醛的摩尔质量为
=15g/mol,最简单的乙醛的摩尔质量为44克/摩尔,故不可能为乙醛、丙醛、丁醛,
若为甲醛,3g甲醛的物质的量为
=0.1mol,完全反应生成Ag的物质的量为0.1mol×4=0.4mol,符合题意,
故选A.
| 43.2g |
| 108g/mol |
若不是甲醛,则醛的物质的量为
| 0.4mol |
| 2 |
| 3g |
| 0.2mol |
若为甲醛,3g甲醛的物质的量为
| 3g |
| 30g/mol |
故选A.
点评:本题考查有机物推断,难度中等,注意掌握醛与银氨溶液反应中醛基与Ag的物质的量关系.

练习册系列答案
相关题目
以下所述事实与化学(或离子)方程式不相符的是( )
| A、NH3结合H+能力比H2O强:NH3+H3O+═NH4++H2O |
| B、向NaHSO4溶液中加入Ba(OH)2溶液至中性:2H++SO42-+Ba2++2OH-═2H2O+BaSO4↓ |
| C、能说明盐酸是强酸:HCl+AgNO3═AgCl↓+HNO3 |
| D、氨水中通入少量SO2气体:2NH3?H2O+SO2═2NH4++SO32- |
下列各组物质中,不属于同素异形体的是( )
| A、石墨和金刚石 |
| B、H2O和H2O2 |
| C、O3与O2 |
| D、S2和S8(两种不同硫单质分子) |
在一种一元碱ROH的溶液中,加入一种一元酸HA溶液,当反应后溶液呈现中性,下列判断中一定正确的是( )
| A、加入的一元酸HA过量 |
| B、生成的盐RA不能发生水解 |
| C、加入的酸与碱的物质的量相等 |
| D、反应后溶液中C(A-)=C(R+) |
短周期元素X、Y、Z在元素周期表中的位置如图所示,下列说法正确的是( )
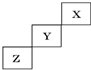

| A、X、Y、Z三种元素中,X的非金属性最强 |
| B、Y的氢化物的稳定性比Z的强 |
| C、Y的最高正化合价为+7价 |
| D、X的单质的熔点比Z的高 |
短周期元素X、Y的原子序数相差2,下列有关叙述正确的是( )
| A、X与Y不可能位于同一主族 |
| B、X与Y一定位于同一周期 |
| C、X与Y可能形成共价化合物XY |
| D、X与Y可能形成离子化合物XY |
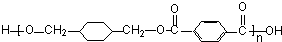
 -CH3+Cl2→
-CH3+Cl2→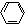 -CH2Cl+HCl
-CH2Cl+HCl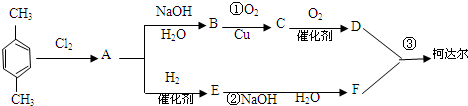
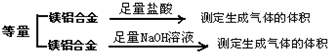
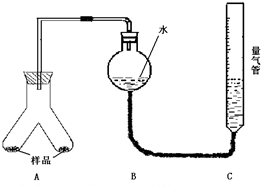 为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究.请回答下列问题:
为测定镁铝合金(不含其它元素)中铝的质量分数,甲乙两个学习小组设计了下列二种不同的实验方案进行探究.请回答下列问题: