题目内容
8. 已知:①图中每个小三角形的三种物质中至少含有一种相同元素,H与I含有完全相同的元素.②A、J为固体单质,D为气体单质,其余物质为常见化合物.③B为淡黄色化合物,B与H反应能生成D.④E为常见金属氧化物.⑤F的溶液和H反应生成白色胶状沉淀G.
已知:①图中每个小三角形的三种物质中至少含有一种相同元素,H与I含有完全相同的元素.②A、J为固体单质,D为气体单质,其余物质为常见化合物.③B为淡黄色化合物,B与H反应能生成D.④E为常见金属氧化物.⑤F的溶液和H反应生成白色胶状沉淀G.根据以上信息,回答下列问题:
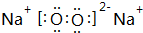
(1)物质B的电子式为
 .
.(2)写出B与H反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
(3)向F水溶液中通入少量H生成G,该反应的离子方程式为2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-.
(4)写出由E转化成D的化学反应式(注明必要的反应条件)2Al2O3(融融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;若反应中有100g D单质生成,则转移电子数目为12.5NA.
(5)若测得1g固体单质J与一定量的气体H恰好完全反应生成气态I时吸收的热量为Q kJ,则该反应的热化学方程式可表示为C(s)+CO2(g)═2CO(g)△H=+12QkJ•mol-1.
分析 B为淡黄色化合物,B与H反应能生成D,且D为气体单质,则B为Na2O2,D为O2,H为H2O或CO2;A为固体单质,A能够发生反应生成Na2O2,则A为金属Na;Na和过氧化钠都能够转化成C,则C为NaOH;J为固体单质,J能够转化成H,则J为C,又H与I含有完全相同的元素,则H为CO2,I为CO;E为常见金属氧化物、⑤F的溶液和H反应生成白色胶状沉淀G,则F为NaAlO2,G为Al(OH)3,E为Al2O3,电解融融的E(Al2O3)可得铝和氧气,据此进行解答.
解答 解:B为淡黄色化合物,B与H反应能生成D,且D为气体单质,则B为Na2O2,D为O2,H为H2O或CO2;A为固体单质,A能够发生反应生成Na2O2,则A为金属Na;Na和过氧化钠都能够转化成C,则C为NaOH;J为固体单质,J能够转化成H,则J为C,又H与I含有完全相同的元素,则H为CO2,I为CO;E为常见金属氧化物、⑤F的溶液和H反应生成白色胶状沉淀G,则F为NaAlO2,G为Al(OH)3,E为Al2O3,电解融融的E(Al2O3)可得铝和氧气,
(1)B为Na2O2,过氧化钠为离子化合物,其电子式为 ,
,
故答案为: ;
;
(2)B为过氧化钠,H为二氧化碳,过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2=2Na2CO3+O2,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(3)向偏铝酸钠的水溶液中通入少量二氧化碳生成氢氧化铝沉淀和碳酸钠,反应的离子方程式为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,
故答案为:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-;
(4)E为氧化铝,电解融融的氧化铝可以获得铝和氧气,反应的化学方程式为:2Al2O3(融融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;100g氧气的物质的量为:$\frac{100g}{32g/mol}$=3.125mol,根据电子守恒,生成3.125mol氧气转移的电子的物质的量为:3.125mol×4=12.5mol,所以转移的电子数为12.5NA,
故答案为:2Al2O3(融融)$\frac{\underline{\;电解\;}}{\;}$4Al+3O2↑;12.5NA;
(5)若测得1g固体单质J与一定量的气体H恰好完全反应生成气态I时吸收的热量为Q kJ,J为C,H为二氧化碳,I为CO,1g C的物质的量为:$\frac{1g}{12g/mol}$=$\frac{1}{12}$mol,则1molC完全反应吸收的热量为12QkJ,故该反应的热化学方程式为:C(s)+CO2(g)═2CO(g)△H=+12Q kJ•mol-1,
故答案为:C(s)+CO2(g)═2CO(g)△H=+12Q kJ•mol-1.
点评 本题考查无机物的推断,题目难度中等,“B为淡黄色固体、A、J为固体单质,D为气体单质”等为解答本题的突破口,熟悉物质的性质及相互转化推断物质为解答本题的关键,侧重Na、C、Al元素单质及其化合物性质的考查,试题充分培养了学生的分析、理解能力及逻辑推理能力.

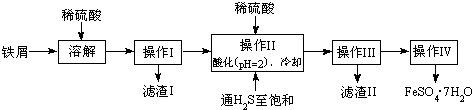
查询资料,得有关物质的数据如表:
| 25℃时 | pH值 |
| 饱和H2S溶液 | 3.9 |
| SnS沉淀完全 | 1.6 |
| FeS开始沉淀 | 3.0 |
| FeS沉淀完全 | 5.5 |
(2)操作II中,通入硫化氢至饱和的目的是:①除去溶液中的Sn2+离子;②防止Fe2+被氧化;③在溶液中用硫酸酸化至pH=2的目的是防止Fe2+离子生成沉淀.
(3)操作IV的顺序依次为蒸发浓缩、冷却结晶、过滤洗涤.
(4)操作IV得到的绿矾晶体用少量冰水洗涤,其目的是:①除去晶体表面附着的硫酸等杂质;②降低洗涤过程中FeSO4•7H2O的损耗.
(5)已知常温下,Ksp[Fe(OH)2]=1.64×10-14,则求得反应:Fe2++2H2O?Fe(OH)2+2H+的平衡常数为:0.6×10-14(保留1位小数)
(6)测定绿矾产品中Fe2+含量的方法是:a.称取2.850g绿矾产品,溶解,在250mL容量瓶中定容;b.量取25.00mL待测溶液于锥形瓶中;c.用硫酸酸化的0.01000mol/LKMnO4溶液滴定至终点,消耗KMnO4溶液体积的平均值为20.00mL.计算上述样品中FeSO4•7H2O的质量分数为97.5%.(保留3位小数)
| A. | 离子化合物中只存在离子键 | |
| B. | 非金属元素组成的化合物中可能存在离子键 | |
| C. | 由不同种元素组成的多原子分子里,一定只存在极性共价键 | |
| D. | 含金属元素的化合物中一定存在离子键 |
| A. | 升高温度 | B. | 降低压强 | C. | 使用催化剂 | D. | 及时分离出氨气 |
| 醋酸浓度/mol•L-1 | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(1)写出醋酸的电离方程式:CH3COOH?CH3COO-+H+.
(2)醋酸溶液中存在的微粒有H2O、CH3COOH、CH3COO-、H+、OH-.
(3)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是当醋酸浓度为0.001mol/L时,溶液中的氢离子浓度小于0.001mol/L.
(4)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度(选填“增大”“减小”或“不变”)增大.
(5)常温常压下,在 pH=5的稀醋酸溶液中,c(CH3COO-)=(10-5-10-9)mol/L (精确值,用表达式表示).
(6)下列方法中,可以使0.10mol•L-1CH3COOH溶液中CH3COOH电离程度增大的是de.
a.加入少量0.10mol•L-1的稀盐酸 b.加入少量冰醋酸
c.加入少量氯化钠固体 d.加热CH3COOH溶液
e.加入Zn粒 f.加入少量0.10mol•L-1的CH3COONa溶液.
| A. | 18.4mol | B. | 18.4mol•L-1 | C. | 20.4 | D. | 20.4mol•L-1 |
 一定质量的镁、铝混合物投入2mol•L-1的盐酸中,待金属完全溶解后,向溶液中加入2mol•L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则n(Mg)/n(Al)的最大值是( )
一定质量的镁、铝混合物投入2mol•L-1的盐酸中,待金属完全溶解后,向溶液中加入2mol•L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示.则n(Mg)/n(Al)的最大值是( )| A. | 1:1 | B. | 8:1 | C. | 4:1 | D. | 5:2 |
| A. | 32g/mol | B. | 64 | C. | 64g/mol | D. | 4g |