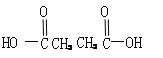��Ŀ����
����Ŀ��A��B��C��D��E���ֶ�����Ԫ�أ����ǵ�ԭ��������������AԪ��������ԭ���а뾶��С��ԭ�ӣ�BԪ�ص�����������Ӧˮ���������⻯������һ����X��D��Aͬ���壬����Eͬ���ڣ�EԪ�ص��������������������������3/4��A��B��D��E������Ԫ���У�ÿһ�ֶ�����CԪ���γ�ԭ�Ӹ����Ȳ���ͬ�Ļ����
��ش���������:
��1��A��C��Ԫ���γɵ�ԭ�Ӹ�����Ϊ1:1�Ļ�����û��������ʽΪ ��
��2��BԪ�ص��⻯���ڴ������ڵ��������CԪ�ص��ʷ�Ӧ�Ļ�ѧ����ʽΪ ��
��3��X��ˮ��Һ�� �������ԡ����Ի����ԣ���ԭ���� �������ӷ���ʽ��ʾ����
��4��C��E��Ԫ����Ƚϣ��ǽ����Խ�ǿ���� ������Ԫ������������������֤�ý��۵��� ���������������
A���Ƚ�������Ԫ������̬�⻯��ķе�
B���Ƚ�������Ԫ�صĵ����ڳ����µ�״̬
C���Ƚ�������Ԫ�ص���̬�⻯����ȶ���
D���Ƚ�������Ԫ�صĵ������������ϵ�����
��5��C��D��Ԫ���γɵ�ԭ�Ӹ�����Ϊ1:1�Ļ����E��C��Ԫ���γɵ�ԭ�Ӹ�����Ϊ1:2�Ļ���������ֻ����ﷴӦ�Ļ�ѧ����ʽΪ ��
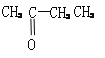
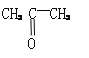
��6��A��C��A��E�ɷֱ��γɼס������ָ�һ��˫ԭ�����ӣ��Ҽ���10�����ӣ�����18�����ӣ�������ҷ�Ӧ�����ӷ���ʽΪ ��
���𰸡���1��![]() ����2�� 4NH3��5O2
����2�� 4NH3��5O2![]() 4NO��6H2O����3�����ԣ�NH4++H2O
4NO��6H2O����3�����ԣ�NH4++H2O![]() NH3.H2O+H+����4������ CD����5��Na2O2+SO2=Na2SO4����6��HS����OH��=S2����H2O��
NH3.H2O+H+����4������ CD����5��Na2O2+SO2=Na2SO4����6��HS����OH��=S2����H2O��
����������������� A�뾶����С�ģ��Ƴ�AΪH��BԪ�ص�����������Ӧˮ���������⻯������һ���Σ���BΪN��XΪNH4NO3��E��������Ǵ�����������3/4����EΪS��D��Hͬ�壬��Eͬ���ڣ���DΪNa��A��B��D��E������Ԫ���У�ÿһ�ֶ�����CԪ���γ�ԭ�Ӹ����Ȳ���ͬ�Ļ�����Ƴ�CΪO����1��H��O�γ�1��1�Ļ�������H2O2�������ʽΪ��![]() ����2��B���⻯����NH3���ڴ��������º�������Ӧ���仯ѧ��Ӧ����ʽΪ��4NH3��5O2
����2��B���⻯����NH3���ڴ��������º�������Ӧ���仯ѧ��Ӧ����ʽΪ��4NH3��5O2![]() 4NO��6H2O����3��XΪNH4NO3������ǿ�������Σ�ˮ��Һ�����ԣ�����ΪNH4������ˮ�⣬c��H������c��OH������NH4++H2O
4NO��6H2O����3��XΪNH4NO3������ǿ�������Σ�ˮ��Һ�����ԣ�����ΪNH4������ˮ�⣬c��H������c��OH������NH4++H2O![]() NH3.H2O+H+����4��O��S����ͬһ���壬���ϵ��£��ǽ����Լ�����O��S��A���ǽ������ǻ�ѧ���ʣ��е����������ʣ��ʴ���B�������µ�״̬������˵���ǽ����Ե�ǿ�����ʴ���C���ǽ�����Խǿ�����⻯��Խ�ȶ�������ȷ��D���ǽ�����Խǿ��������ӦԽ���ף�����ȷ����5��C��D�γ�1��1�Ļ�����ΪNa2O2��E��C�γ�1��2�Ļ�����ΪSO2��Na2O2����ǿ�����ԣ�SO2���л�ԭ�ԣ����߷���������ԭ��Ӧ��Na2O2+SO2=Na2SO4����6��������Ϣ����ΪOH������ΪHS�������������ӷ�Ӧ�ǣ�HS����OH��=S2����H2O��
NH3.H2O+H+����4��O��S����ͬһ���壬���ϵ��£��ǽ����Լ�����O��S��A���ǽ������ǻ�ѧ���ʣ��е����������ʣ��ʴ���B�������µ�״̬������˵���ǽ����Ե�ǿ�����ʴ���C���ǽ�����Խǿ�����⻯��Խ�ȶ�������ȷ��D���ǽ�����Խǿ��������ӦԽ���ף�����ȷ����5��C��D�γ�1��1�Ļ�����ΪNa2O2��E��C�γ�1��2�Ļ�����ΪSO2��Na2O2����ǿ�����ԣ�SO2���л�ԭ�ԣ����߷���������ԭ��Ӧ��Na2O2+SO2=Na2SO4����6��������Ϣ����ΪOH������ΪHS�������������ӷ�Ӧ�ǣ�HS����OH��=S2����H2O��

����Ŀ����1���о�NO2��SO2��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣 ��֪��
2SO2(g)+O2(g) 2SO3(g) ��H= -196.6kJ��mol��1
2NO(g)+O2(g)![]() 2NO2(g) ��H= -113.0kJ��mol-1
2NO2(g) ��H= -113.0kJ��mol-1
��ӦNO2(g)+SO2(g)![]() SO3(g)+NO(g)����H= kJ��mol-1
SO3(g)+NO(g)����H= kJ��mol-1
��2�����Ƕ�ֲ����������ȱ�ٵ�Ԫ�أ��ϳɰ��ķ�Ӧ����������ʳ�����Ӧ���£�
N2(g)��3H2(g)![]() 2NH3(g)��
2NH3(g)��
��һ�������£���һ������N2��H2�Ļ���������ij�����ܱ������У�һ��ʱ�������������˵���÷�Ӧ�ﵽƽ��״̬���� ������ţ���
A�������л��������ܶȲ���ʱ��仯 |
B������3 mol H-H����ͬʱ�γ�6 mol N-H�� |
C��N2��H2��NH3�����ʵ���֮��Ϊ1:3:2 |
D�������е�ѹǿ����ʱ��仯 |
��3����25 ����101 kPa�£�1 g�״�ȼ������CO2��Һ̬ˮʱ����22.68 kJ����÷�Ӧ���Ȼ�ѧ����ʽ��____________��
����Ŀ���±���ʵ�����Ʊ�������й����ݣ�
��� | ʵ������ | ʵ��ԭ�� | ���巢��װ�� |
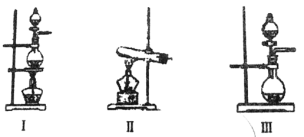
�� | �Ʊ����� | H2O2��O2 | __________________ |
�� | �Ʊ��������� | Na2SO3��SO2 | __________________ |
�� | �Ʊ����� | HCl��Cl2 | __________________ |
��1�����������д��Ʊ����̿�������ѡ����ʵ�����������ʵ�ֵ���__________________(������Ļ�ѧʽ����ͬ)���ӷ�Ӧԭ���������Բ�ͬ�����������������__________________��
��2�����ݱ�������ʵ��ԭ����������װ����ѡ����ʵ����巢��װ�ã������������ϱ��еĿո��С�
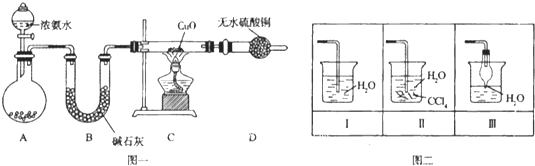
��3��ijѧϰС���������ͼʵ�飬����������ͨ������װ������֤���������ʣ�

��ͨ��������A�е�������__________________������ʵ��װ�ô��ڵ�����ȱ����__________________��
��Cװ���з�����Ӧ�����ӷ���ʽΪ__________________��
����С��ͬѧ�����һ��ʵ�飬֤��ϴ��ƿB�е�Na2SO3�����������������Ϊ��ȡһ������B����Һ��һ�ྻ���Թ��У������м��������ữ�����ᱵ��Һ����������ɫ������֤���Ѿ�������������Ϊ__________________ (����������������)����?