题目内容
14.有甲、乙、丙三种元素,甲元素M层的电子数是其K层的电子数的$\frac{1}{2}$,乙元素原子核内无中子,丙元素原子核内有8个质子.(1)依次写出甲、乙、丙三种元素的元素名称:甲钠、乙氢、丙氧
(2)画出甲、乙、丙三种元素形成的化合物的电子式和丙离子的结构示意图:化合物
 、丙
、丙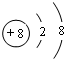 .
.
分析 有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的$\frac{1}{2}$,其M层电子数为1,则甲为Na;乙元素原子核内无中子,则乙为H;丙元素原子核内有8个质子,则丙为O;据此解答.
解答 解:有甲、乙、丙、丁四种元素,甲元素M层的电子数是其K层的电子数的$\frac{1}{2}$,其M层电子数为1,则甲为Na;乙元素原子核内无中子,则乙为H;丙元素原子核内有8个质子,则丙为O;
(1)由上述分析可知,甲、乙、丙、丁四种元素的元素符号分别为:Na,H,O,
故答案为:钠;氢;氧;
(2)甲、乙、丙三种元素形成的化合物是氢氧化钠,其电子式为:NaOH的电子式: ,丙离子为O2-离子的结构示意图为
,丙离子为O2-离子的结构示意图为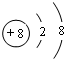 ,故答案为:
,故答案为: ;
;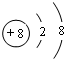 .
.
点评 本题考查原子结构与元素性质,比较基础,侧重对基础知识的巩固.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
5.下列叙述错误的是( )
| A. | 1mol任何物质都含有6.02×1023个原子 | |
| B. | 0.012kg12C 含有阿伏加德罗常数个碳原子 | |
| C. | 在使用摩尔表示物质的量的单位时,应指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
2.仪器名称为“容量瓶”的是( )
| A. | 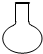 | B. |  | C. | 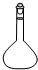 | D. |  |
9.由NO与NO2组成的混合气体中氮元素的质量分数为$\frac{35}{91}$,则混合气体中NO与NO2的体积比为( )
| A. | 1:1 | B. | 2:3 | C. | 3:2 | D. | 35:56 |
19.已知HA、H2B为二种弱酸,HA的电离常数为KHA,H2B的电离常数为K1、K2,其大小依次是K1>KHA>K2,由此可以推测以下各反应中不能进行的是( )
| A. | NaA+H2B→NaHB+HA | B. | 2NaA+H2B→Na2B+2HA | ||
| C. | NaHB+HA→NaA+H2B | D. | Na2B+HA→NaHB+NaA |
6.含下列某种杂质的氯化钠样品,经测定氯的质量分数为62.0%,则该样品中含有的杂质可能是( )
| A. | MgCl2 | B. | ZnCl2 | C. | BaCl2 | D. | KCl |
3.下列与化学概念有关的说法正确的是( )
| A. | 化合反应均为氧化还原反应 | B. | 金属氧化物均为碱性氧化物 | ||
| C. | 烧碱、纯碱、熟石灰都是碱 | D. | BaSO4、NaOH、HNO3都是强电解质 |
