题目内容
14.下列化学用语的表示中,正确的是( )| A. | 氢负离子(H-)结构示意图  | B. | HF的电子式 | ||
| C. | 氮气的结构式: | D. | NH3的电子式 |
分析 A.氢负离子有1个电子层,核外电子数为2;
B.氟化氢为共价化合物,分子中不存在阴阳离子;
C.氮气的结构式中不需要标出未成键电子对;
D.氨气的电子式中漏掉了氮气的一对未成键电子对.
解答 解:A.氢负离子有1个电子层,核外电子数为2,离子结构示意图为 ,故A正确;
,故A正确;
B.氟化氢为共价化合物,氟化氢正确的电子式为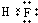 ,故B错误;
,故B错误;
C.氮气分子中含有氮氮三键,氮气正确的结构式为:N≡N,故C错误;
D.NH3属于共价化合物,不存在离子键,分子中存在3对共用电子对,氮原子最外层为8个电子,氨气的电子式为 ,故D错误;
,故D错误;
故选A.
点评 本题考查了化学用语的表示方法,题目难度中等,涉及离子结构示意图、电子式、结构式等知识,明确常见化学用语的概念及书写原则为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
4.下列物质中属于电解质的是( )
| A. | 氯化钠晶体 | B. | 酒精 | C. | 氨气 | D. | 盐酸 |
5.已知:M、N为短周期元素,M的原子序数小于N.M原子的最外层电子数是次外层电子数的3倍,N原子的次外导电子数是最外层电子数的2倍.下列说法中正确的是( )
| A. | 元素M、N属于同周期元素 | B. | 元素M、N属于同主族元素 | ||
| C. | 两元素组成的化合物为共价化合物 | D. | 两元素的原子半径大小:M>N |
2.关于氢键及分子间作用力,下列说法正确的是( )
| A. | 氢键比分子间作用力强,所以它属于化学键 | |
| B. | 分子间形成的氢键使物质的熔点和沸点升高 | |
| C. | 沸点CO2高于CH4是氢键作用所至 | |
| D. | H2O是一种稳定的化合物,这是由于H2O之间形成氢键所致 |
9.下列反应属于放热反应的是( )


| A. | 氢氧化钡晶体和氯化铵晶体的反应 | B. | 能量变化如右图所示的反应 | ||
| C. | 不需要加热就能够发生的反应 | D. | 铁与盐酸的反应 |
19.下列各组离子在指定的环境中一定能大量存在的是( )
| A. | 在pH=1的无色溶液中:K+、Na+、NO3- | |
| B. | 在含碳酸钠的溶液中:NH4+、Fe3+、NO3- | |
| C. | 在能使紫色石蕊试纸变蓝色的溶液中:Na+、Cu2+、S2-、 | |
| D. | 由水电离出的c(H+)=1×10-12 mol•L-1的溶液中:K+、Na+、OH-、 |
6.位于元素周期表第二周期ⅥA族的元素是( )
| A. | Li | B. | O | C. | Al | D. | Cl |
3.下列叙述中能肯定说明金属A比金属B的活泼性强的是( )
| A. | A原子最外层电子数比B原子的最外层电子数少 | |
| B. | 将A与B组成原电池时,A为正极 | |
| C. | 1molA从酸中置换生成的H2比1mol B从酸中置换生成的H2多 | |
| D. | 常温时,A能从酸中置换出氢,而B不能 |
4.光纤通信是一种现代化的通信手段,制造光导纤维的主要原料是( )
| A. | Na2CO3 | B. | CaO | C. | CaCO3 | D. | SiO2 |