题目内容
下图是一套制取并验证氯气部分化学性质的实验装置。
回答下列问题:反应的方程式:MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑
(1)装置A中,仪器a盛有的试剂为__ __。
(2)当Cl2气流通过一段时间后,装置B中溶液的pH值____7(填“>”“<”或“=”),写出Cl2与水反应的方程式
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为_ ___色。
(4)当Cl2气流持续通过时,装置D中干燥的有色布条能否褪色?为什么?
____ ______ __。
(5)装置E的作用是_____ ___。并写出该反应的化学方程式: 。
(6)写出氯气与石灰乳制取漂白粉的化学方程式: ______ ______;
(1) _浓盐酸 _。(2分)
(2) _ < __,(1分) Cl2+H2O≒HCl+HClO (2分)
(3)_ 蓝色 __。(2分)
(4)_ 能,因为湿润的氯气有漂白性 。(2分)
(5) 吸收多余的氯气。(1分) Cl2+2NaOH===NaCl+NaClO+H2O 。(2分)
(6)__2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O_ _;(2分)
解析:

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目

 气部分化学性质的实验装置。
气部分化学性质的实验装置。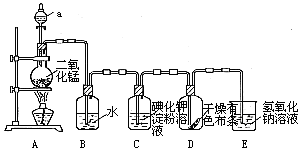
 MnCl2+2H2O+ Cl2↑回答下列问题:
MnCl2+2H2O+ Cl2↑回答下列问题:
 MnCl2+2H2O+ Cl2↑
MnCl2+2H2O+ Cl2↑
 MnCl2+2H2O+
Cl2↑
MnCl2+2H2O+
Cl2↑