题目内容
银锌电池广泛用作各种电子仪器的电源,它的充电和放电过程可以表示为
2Ag+Zn(OH)2
Ag2O+Zn+H2O
此电池充电时,阴极上发生反应的物质是( )
2Ag+Zn(OH)2
| 充电 |
| 放电 |
此电池充电时,阴极上发生反应的物质是( )
| A、Ag |
| B、Zn(OH)2 |
| C、Ag2O |
| D、Zn |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在原电池中,充电时阴极上是失电子发生氧化反应的过程.
解答:
解:在银锌二次电池中,根据反应:2Ag+Zn(OH)2
Ag2O+Zn+H2O,充电时为电解池,阴极上Zn(OH)2失电子发生氧化反应生成Zn,所以充电时,阴极上发生反应的物质是Zn(OH)2.
故选B.
| 充电 |
| 放电 |
故选B.
点评:本题考查原电池知识,侧重于学生的分析能力的考查,注意把握原电池的工作原理,从元素化合价的角度认识物质的变化,把握电极反应,难度不大.

练习册系列答案
相关题目
 某容积可变的密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+B(g)?2C(g)+Q(Q>0),容器中物质浓度随时间变化的曲线如右图所示.下列说法中正确的是( )
某容积可变的密闭容器中充入等物质的量的气体A和B,一定温度下发生反应:A(g)+B(g)?2C(g)+Q(Q>0),容器中物质浓度随时间变化的曲线如右图所示.下列说法中正确的是( )| A、30min时降低温度,40min时升高温度 |
| B、40min~54min之间反应速率v(正)<v(逆) |
| C、设20min和30min时的平衡常数分别为K1和K2,则K1>K2 |
| D、0~8minA的平均反应速率为0.64mol/(L?min) |
下列物质中,与NaOH溶液、Na2CO3、溴水、苯酚钠水溶液和甲醇都能反应的是( )
| A、C6H5OH |
| B、CH2=CH-COOH |
| C、CH3COOH |
| D、CH3CHO |
一定温度下,向饱和Na2SO4溶液中加入ag无水Na2SO4粉末,搅拌、静置后析出bgNa2SO4?10H2O晶体,则bg-ag的值是( )
| A、原饱和溶液中减少的Na2SO4的质量 |
| B、原饱和溶液中失去的水的质量 |
| C、原饱和溶液中失去的水和NaSO4的质量总和 |
| D、析出晶体中含有的Na2SO4的质量 |
镍氢电池(NiMH)目前已经成为混合动力汽车的一种主要电池类型,NiMH中的M表示金属或合金,该电池在充电过程中的总反应方程式是:Ni(OH)2+M═NiOOH+MH
已知:6NiOOH+NH3+H2O+OH-═6Ni(OH)2+NO2-
下列说法正确的是( )
已知:6NiOOH+NH3+H2O+OH-═6Ni(OH)2+NO2-
下列说法正确的是( )
| A、NiMH电池放电过程中,正极的电极反应式为:NiOOH+H2O+e-═Ni(OH)2+OH- |
| B、充电过程中OH-离子从阳极向阴极迁移 |
| C、充电过程中阴极的电极反应式:H2O+M+e-═MH+OH-,H2O中的H被M还原 |
| D、NiMH电池中可以用KOH溶液、氨水等作为电解质溶液 |
A、B属于短周期中不同主族的元素,A、B原子的最外层电子中,成对电子和未成对电子占据的轨道数相等,若A元素的原子序数为a,则B元素的原子序数为( )
| A、a-4 | B、a+1 |
| C、a+3 | D、a+4 |
有关甲醛(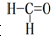 )、苯、二氧化碳及水说法不正确的是( )
)、苯、二氧化碳及水说法不正确的是( )
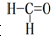 )、苯、二氧化碳及水说法不正确的是( )
)、苯、二氧化碳及水说法不正确的是( )| A、苯与B3N3H6互为等电子体,且分子中原子共平面 |
| B、甲醛、苯和二氧化碳中碳原子均采用sp2杂化 |
| C、苯、二氧化碳是非极性分子,水和甲醛是极性分子 |
| D、水的沸点比甲醛高得多,是因为水分子间能形成氢键,而甲醛分子间不能形成氢键 |
下列有关溶液组成的描述合理的是( )
| A、无色溶液中可能大量存在Al3+、NH4+、Cl-、S2- |
| B、酸性溶液中可能大量存在Na+、ClO-、SO42-、I- |
| C、弱碱性溶液中可能大量存在Na+、K+、Cl-、HCO3- |
| D、中性溶液中可能大量存在Fe3+、K+、Cl-、SO42- |