��Ŀ����
�ݱ�������һ�ֽ�Thibacillus Ferroxidans��ϸ�������������µ�������Һ�У��ܽ���ͭ��CuFeS2�������������Σ������ķ�ӦΪ��
4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2��SO4��3+2H2O
��1��CuFeS2��Fe�Ļ��ϼ�Ϊ+2��������Ӧ�б�������Ԫ����______��
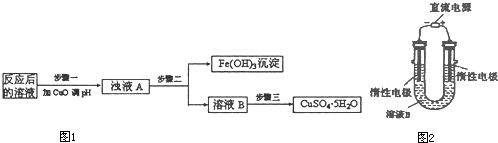
��2����ҵ����������������Ӧ�����Һ������������ͼ1���Ʊ�������CuSO4?5H2O����
�ٷ������б�������KSP����Ӧ������������ij����ܽ�ƽ�ⳣ������
| Ksp | �������↑ʼ����ʱ��pH | �������������ȫʱ��pH | |
| Fe3+ | 2.6��10-39 | 1.9 | 3.2 |
| Cu2+ | 2.2��10-20 | 4.7 | 6.7 |
�ڲ������еľ������������______��
��3�����������������ͼ2��װ�ô���ҺB����������ͭ���ù������ұߵ缫�ķ�Ӧʽ��______���ܷ�Ӧ�ķ���ʽ��______��
��4����ҵ��ұ��ͭ�ķ���֮һΪ��Cu2S��s��+2Cu2O��s��=6Cu��s��+SO2��g����H
��֪����2Cu��s��+
 O2��g��=Cu2O��s����H=-12kJ?mol-1
O2��g��=Cu2O��s����H=-12kJ?mol-1��2Cu��s��+S��s��=Cu2S��s����H=-79.5kJ?mol-1
��S��s��+O2��g��=SO2��g����H=-296.8kJ?mol-1
��÷�ұ��ͭ�ķ�Ӧ�С�H=______��
�⣺��1����4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2��SO4��3+2H2O��Ӧ�У�CuFeS2��Fe��+2�۱�Ϊ�����е�+3�ۣ����-2�۱�Ϊ�����е�+6�ۣ�Fe��CuFeS2�е�S���ϼ����ߣ��ڷ�Ӧ�б�������
�ʴ�Ϊ��Fe��CuFeS2�е�S��
��2���ٸ�ʵ���Ŀ�����Ʊ�������CuSO4?5H2O�������ȥ�������������ӣ����Ե�����Һ��pHʹ���������ӱ���������������ҳ�����ȫ����ͭ���Ӳ��ܳ��������Բ���һӦ������Һ��pH��Χ��3.2��pH��4.7������CuO��CuO��H+��Ӧʹc��H+����С��c��OH-������ʹ��Һ��c��Fe3+��?c3��OH-����Ksp[Fe��OH��3]������Fe3+���ɳ�������ȥ��
�ʴ�Ϊ��3.2��pH��4.7������CuO��H+��Ӧʹc��H+����С��c��OH-������ʹ��Һ��c��Fe3+��?c3��OH-����Ksp[Fe��OH��3]������Fe3+���ɳ�������ȥ��
��CuSO4�ܽ�����¶�Ӱ��ϴ�����ͭ��Һ����Ũ�����ȵ�����ͭ��Һ���ò��������£��õ�����ͭ���壬
�ʴ�Ϊ������Ũ������ȴ�ᾧ��
��3��CuSO4��Һ��ͭ���ӵķŵ��������������ӵķŵ�����������ͭ�����ȷŵ磻���������ӵķŵ�����������������ӵķŵ������������������ȷŵ磬������ʧ���ӣ�����������Ӧ�����Ըù������ұߵ缫������������������ʧ������������4OH--4e-=O2��+2H2O�������ϵõ��ӣ���Ӧ��ԭ��Ӧ������ͭ���ӵ������ϵõ�������ͭCu2++2e-=Cu���ܵķ�ӦΪ��2CuSO4+2H2O 2Cu+2H2SO4+O2����
2Cu+2H2SO4+O2����
�ʴ�Ϊ��4OH--4e-=O2��+2H2O��2CuSO4+2H2O 2Cu+2H2SO4+O2����
2Cu+2H2SO4+O2����
��4����2Cu��s��+ O2��g��=Cu2O��s����H=-12kJ?mol-1��2Cu��s��+S��s��=Cu2S��s����H=-79.5kJ?mol-1��S��s��+O2��g��=SO2��g����H=-296.8kJ?mol-1���ݸ�˹���ɢ�-�١�2-�ڿɵ�Cu2S��s��+2Cu2O��s��=6Cu��s��+SO2��g������H4=-193.33kJ/mol��
O2��g��=Cu2O��s����H=-12kJ?mol-1��2Cu��s��+S��s��=Cu2S��s����H=-79.5kJ?mol-1��S��s��+O2��g��=SO2��g����H=-296.8kJ?mol-1���ݸ�˹���ɢ�-�١�2-�ڿɵ�Cu2S��s��+2Cu2O��s��=6Cu��s��+SO2��g������H4=-193.33kJ/mol��
�ʴ�Ϊ��-193.3kJ?mol-1��
��������1����������ԭ��Ӧ�У����ϼ����ߵ�Ԫ���ڷ�Ӧ�б�������
��2���ٸ���ʵ���Ŀ�Ľ����Ӧ������������ij����ܽ�ƽ�ⳣ�����н�����ó����ܽ�ƽ���ƶ���ԭ�����н��
���ܽ�����¶�Ӱ��ϴ�����ʴ���Һ�нᾧ�����ķ�������ȴ�ȱ�����Һ��
��3����ҺBΪ����ͭ������ҺB����������ͭ��ʵ����2CuSO4+2H2O 2Cu+2H2SO4+O2����
2Cu+2H2SO4+O2����
��4�����ݸ�˹���ɼ��㷴Ӧ�ȣ�
������������Ҫ�����Ʊ���������������ͼ���ͭ���仯����������ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�
�ʴ�Ϊ��Fe��CuFeS2�е�S��
��2���ٸ�ʵ���Ŀ�����Ʊ�������CuSO4?5H2O�������ȥ�������������ӣ����Ե�����Һ��pHʹ���������ӱ���������������ҳ�����ȫ����ͭ���Ӳ��ܳ��������Բ���һӦ������Һ��pH��Χ��3.2��pH��4.7������CuO��CuO��H+��Ӧʹc��H+����С��c��OH-������ʹ��Һ��c��Fe3+��?c3��OH-����Ksp[Fe��OH��3]������Fe3+���ɳ�������ȥ��
�ʴ�Ϊ��3.2��pH��4.7������CuO��H+��Ӧʹc��H+����С��c��OH-������ʹ��Һ��c��Fe3+��?c3��OH-����Ksp[Fe��OH��3]������Fe3+���ɳ�������ȥ��
��CuSO4�ܽ�����¶�Ӱ��ϴ�����ͭ��Һ����Ũ�����ȵ�����ͭ��Һ���ò��������£��õ�����ͭ���壬
�ʴ�Ϊ������Ũ������ȴ�ᾧ��
��3��CuSO4��Һ��ͭ���ӵķŵ��������������ӵķŵ�����������ͭ�����ȷŵ磻���������ӵķŵ�����������������ӵķŵ������������������ȷŵ磬������ʧ���ӣ�����������Ӧ�����Ըù������ұߵ缫������������������ʧ������������4OH--4e-=O2��+2H2O�������ϵõ��ӣ���Ӧ��ԭ��Ӧ������ͭ���ӵ������ϵõ�������ͭCu2++2e-=Cu���ܵķ�ӦΪ��2CuSO4+2H2O
 2Cu+2H2SO4+O2����
2Cu+2H2SO4+O2�����ʴ�Ϊ��4OH--4e-=O2��+2H2O��2CuSO4+2H2O
 2Cu+2H2SO4+O2����
2Cu+2H2SO4+O2������4����2Cu��s��+
 O2��g��=Cu2O��s����H=-12kJ?mol-1��2Cu��s��+S��s��=Cu2S��s����H=-79.5kJ?mol-1��S��s��+O2��g��=SO2��g����H=-296.8kJ?mol-1���ݸ�˹���ɢ�-�١�2-�ڿɵ�Cu2S��s��+2Cu2O��s��=6Cu��s��+SO2��g������H4=-193.33kJ/mol��
O2��g��=Cu2O��s����H=-12kJ?mol-1��2Cu��s��+S��s��=Cu2S��s����H=-79.5kJ?mol-1��S��s��+O2��g��=SO2��g����H=-296.8kJ?mol-1���ݸ�˹���ɢ�-�١�2-�ڿɵ�Cu2S��s��+2Cu2O��s��=6Cu��s��+SO2��g������H4=-193.33kJ/mol���ʴ�Ϊ��-193.3kJ?mol-1��
��������1����������ԭ��Ӧ�У����ϼ����ߵ�Ԫ���ڷ�Ӧ�б�������
��2���ٸ���ʵ���Ŀ�Ľ����Ӧ������������ij����ܽ�ƽ�ⳣ�����н�����ó����ܽ�ƽ���ƶ���ԭ�����н��
���ܽ�����¶�Ӱ��ϴ�����ʴ���Һ�нᾧ�����ķ�������ȴ�ȱ�����Һ��
��3����ҺBΪ����ͭ������ҺB����������ͭ��ʵ����2CuSO4+2H2O
 2Cu+2H2SO4+O2����
2Cu+2H2SO4+O2������4�����ݸ�˹���ɼ��㷴Ӧ�ȣ�
������������Ҫ�����Ʊ���������������ͼ���ͭ���仯����������ǽ��Ĺؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
�����Ŀ
��֪�ڳ����£����Ũ�Ⱦ�Ϊ0.1mol/L������������Һ��pH��
| ���� | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
- A.CO32-+C6H5OH��HCO3-+C6H5O-
- B.CO2+H2O+ClO-��HCO3-+HClO
- C.CO2+H2O+C6H5O-��HCO3-+C6H5OH
- D.CO2+H2O+2C6H5O-��CO32-+2C6H5OH

 8SO2+2Fe2O3���÷�Ӧ�б�������Ԫ����______����Ԫ�ط��ţ������÷�Ӧת��2.75mol����ʱ�����ɵĶ��������ڱ�״���µ����Ϊ______L��
8SO2+2Fe2O3���÷�Ӧ�б�������Ԫ����______����Ԫ�ط��ţ������÷�Ӧת��2.75mol����ʱ�����ɵĶ��������ڱ�״���µ����Ϊ______L��

