题目内容
下列说法正确的是( )
| A、减少SO2的排放,可以从根本上消除雾霾 |
| B、聚乙烯塑料、合成橡胶、光导纤维和碳纤维都属于有机高分子材料 |
| C、去除锅炉水垢(含CaSO4)时,可先用Na2CO3溶液处理,而后用醋酸溶解 |
| D、粮食酿酒过程中,淀粉水解生成葡萄糖,葡萄糖水解生成乙醇 |
考点:二氧化硫的化学性质,乙酸的化学性质,葡萄糖的性质和用途,有机高分子化合物的结构和性质
专题:化学应用
分析:A、减少二氧化硫排放防止酸雨污染,不能消除雾霾;
B、光导纤维主要成分为二氧化硅,碳纤维是增强塑料;
C、依据沉淀溶解平衡和溶度积分析判断;
D、葡萄糖是单糖不能水解;
B、光导纤维主要成分为二氧化硅,碳纤维是增强塑料;
C、依据沉淀溶解平衡和溶度积分析判断;
D、葡萄糖是单糖不能水解;
解答:
解:A、减少二氧化硫排放防止酸雨污染,不能消除雾霾,故A错误;
B、光导纤维主要成分为二氧化硅,碳纤维是增强塑料,聚乙烯塑料、合成橡胶属于有机高分子材料,故B错误;
C、依据沉淀溶解平衡和溶度积分析判断,当碳酸根离子浓度和钙离子浓度大于溶度积会沉淀钙离子生成碳酸钙沉淀,后用醋酸溶解,故C正确;
D、葡萄糖是单糖不能水解,故D错误;
故选C.
B、光导纤维主要成分为二氧化硅,碳纤维是增强塑料,聚乙烯塑料、合成橡胶属于有机高分子材料,故B错误;
C、依据沉淀溶解平衡和溶度积分析判断,当碳酸根离子浓度和钙离子浓度大于溶度积会沉淀钙离子生成碳酸钙沉淀,后用醋酸溶解,故C正确;
D、葡萄糖是单糖不能水解,故D错误;
故选C.
点评:本题考查了物质性质的分析判断,注意物质组成和性质的理解应用,掌握基础是关键,题目较简单.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
煤化工生产中常研究不同温度下平衡常数、投料比及产率等问题.已知:CO(g)+H2O(g)?H2(g)+CO2(g)的平衡常数随温度的变化如下表:则下列说法错误的是( )
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A、在830℃,等物质的量的CO和H2O反应达到平衡时,CO的转化率为50% |
| B、在500℃时,反应达到平衡后,增大压强,化学平衡常数K减小 |
| C、恒温、恒容条件下,若混合气体的平均相对分子质量一定,不能确定可逆反应是否达到平衡 |
| D、上述正向反应是放热反应 |
用NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、2 mol SO2和1 mol O2 在一定条件下反应,反应后分子总数大于2NA |
| B、25℃时,在pH=2的1.0 L H2SO4溶液中含有H+数目为0.01NA |
| C、在二氧化硅的晶体中,1mol SiO2含有Si-O键数目为4NA |
| D、25mL 18 mol?L-1浓硫酸与足量Zn反应,转移电子数为0.225NA |
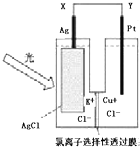 一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)═AgCl(s)=Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e--→Cl-(aq),若将光源移除,电池会立即回复至初始状态.下列说法正确的是( )
一种光化学电池的结构如图,当光照在表面涂有氯化银的银片上时,AgCl(s)═AgCl(s)=Ag (s)+Cl(AgCl),[Cl(AgCl)表示生成的氯原子吸附在氯化银表面],接着Cl(AgCl)+e--→Cl-(aq),若将光源移除,电池会立即回复至初始状态.下列说法正确的是( )| A、光照时,电流由Y流向X |
| B、光照时,Pt电极发生的反应为2Cl-+2e-═Cl2光 |
| C、光照时,Cl-向Ag电极移动 |
| D、光照时,电池总反应为:AgCl(s)+Cu+(aq)═Ag (s)+Cu2+(aq)+Cl-(aq) |
设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A、常温下,1L0.1mol/L的NH4NO3溶液中氮原子数为0.2 NA |
| B、1mol羟基中电子数为10 NA |
| C、2.4g金属镁变为镁离子时失去的电子数为0.1NA |
| D、常温常压下乙烯中C-H键数为4NA |
下列各选项所描述的两个量中,前者一定大于后者的是( )
| A、pH=3的盐酸的Cl-浓度和pH=3的醋酸溶液的CH3COO-浓度 |
| B、pH相同的氨水和醋酸钠溶液中,由水电离产生的c(H+) |
| C、0.1mol/L的盐酸和0.1mol/L的醋酸分别与金属镁反应的速率 |
| D、pH=11的NaOH和pH=11的氨水分别稀释100倍后的pH |