题目内容
(1)埋在地下的输油铁管道,在下列情况下,①在含铁元素较多的酸性土壤中、②在潮湿疏松透气的土壤中、③在干燥致密不透气的土壤中、④在含碳颗粒较多,潮湿透气的中性土壤中.被腐蚀速率最慢的是
(2)以石墨棒为两极,氯化铜溶液为电解液组成的电解池的阴极电极反应式是 在化学反应中发生的能量转变形式是 .
(2)以石墨棒为两极,氯化铜溶液为电解液组成的电解池的阴极电极反应式是
考点:原电池和电解池的工作原理,金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)能形成原电池或发生化学腐蚀的加速铁被腐蚀;
(2)将石墨作电极,电解氯化铜溶液时,阳极上氯离子放电,阴极上铜离子放电,该装置为电解池.
(2)将石墨作电极,电解氯化铜溶液时,阳极上氯离子放电,阴极上铜离子放电,该装置为电解池.
解答:
解:(1)能形成原电池或发生化学腐蚀的加速铁被腐蚀,①中溶液呈酸性,能和铁发生化学腐蚀,②中铁、碳和电解质溶液能构成原电池,铁易失电子作负极而加速被腐蚀,③中不能形成原电池,且没有能腐蚀铁的物质,所以铁不易被腐蚀,④中铁和碳、电解质溶液能构成原电池,铁易失电子而作负极,加速铁被腐蚀,所以腐蚀速率最慢的是③,故选③;
(2)将石墨作电极,电解氯化铜溶液时,阳极上氯离子放电,阴极上铜离子放电,电极反应式为Cu2++2e-═Cu,该装置是将电能转化为化学能的装置,为电解池,故答案为:Cu2++2e-═Cu;电能转化为化学能.
(2)将石墨作电极,电解氯化铜溶液时,阳极上氯离子放电,阴极上铜离子放电,电极反应式为Cu2++2e-═Cu,该装置是将电能转化为化学能的装置,为电解池,故答案为:Cu2++2e-═Cu;电能转化为化学能.
点评:本题考查了原电池和电解池原理,明确原电池构成条件及电解池中离子放电顺序是解本题关键,属于基础题,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质互称为同素异形体的是( )
| A、H2O和H2O2 |
| B、Na2O和Na2O2 |
| C、HClO和HClO |
| D、O2和O3 |
下列各组离子在溶液中能大量共存的是( )
| A、Na+、Fe3+、I-、SCN- |
| B、H+、NH4+、NO3-、CH3COO- |
| C、K+、Ba2+、Cl-、Br- |
| D、Ag+、NO3-、CO32-、Al3+ |
设NA为阿伏加德罗常数的值,下列说法错误的是( )
| A、7.8 g Na2O2与足量的CO2反应,转移的电子数为0.2NA |
| B、36 g重氧(18O2)气体所含分子数为NA,标准状况下的体积约为22.4 L |
| C、17 g氢氧根离子含有的电子数为10NA |
| D、500 mL 0.1 mol?L-1的Al2(SO4)3溶液中,Al3+数小于0.1NA |
下列离子方程式正确的是( )
| A、碳酸氢钠的电离:NaHCO3=Na++HCO3- |
| B、将金属钠加入水中:Na+2H2O=Na++2OH-+H2↑ |
| C、硫化钠水解:S2-+2H2O=H2S↑+2OH- |
| D、向氯化铝溶液中加入过量的氨水:Al3++4OH-=Al(OH )4- |
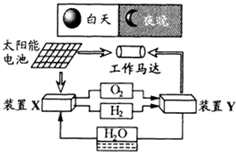 如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )
如图是一种航天器能量储存系统原理示意图.下列说法正确的是( )| A、二氧化硅是太阳能电池的光电转换材料 |
| B、装置Y中正极的电极反应式为:O2+2H2O+4e-=4OH- |
| C、装置X能实现燃料电池的氢气和氧气再生 |
| D、装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
