��Ŀ����
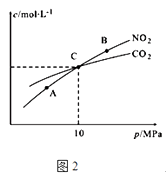
����Ŀ������Һ��Cl2����������������Cl2+SO2+2H2O��2HCl+H2SO4����ͼ���йض����������ʵ�ʵ��װ��ͼ���Իش�����������
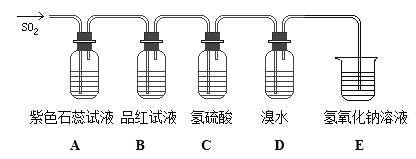
��1��A��B��C��D�ĸ�װ���з���������������________________��________________��_________________��__________________��
��2������������У���Ư���� ����������������� �ۻ�ԭ�� �������ԡ�����ͼ����װ���ж�Ӧ���ֳ��������ǣ�����ţ�
A��_______________B��______________C��________________D��________________��
��3��ʵ����ϣ���B����Һȡ�������Թ��У����ȣ�������_______________��ԭ���ǣ�________________________________��
��4��ʵ����ϣ�ȡ����D����Һ���Թ��У�����BaCl2��Һ��ϡ���ᣬ�����ǣ�_______________________________________________��
��5��E�з�����Ӧ�Ļ�ѧ����ʽΪ____________________________________________��
��6������һ����ʵ֤��Cl�ķǽ����Ա�Sǿ___________________________________��
���𰸡� A����ɫʯ����ɫ B��Ʒ����ɫ C�в�������ɫ����/���� D����ˮ��ɫ �� �� �� �� ��Һ�ָ���ɫ SO2Ư���Ծ����Ȳ��ȶ��� ������ɫ���� 2NaOH+SO2=Na2SO3+H2O ��H2S+ Cl2= 2HCl+ S �����ֱ��������
�������� (1) SO2+H2O![]() H2SO3,ʯ����������SO2�� Ư �� ����Ʒ �� �� ɫ��2H2S+SO2=3S��+2
H2SO3,ʯ����������SO2�� Ư �� ����Ʒ �� �� ɫ��2H2S+SO2=3S��+2
H2O���� ɫ �� ����Br2+2H2O+SO2=2HBr+H2SO4���� ˮ �� ɫ����ȷ��Ϊ��A����ɫʯ����ɫ��B��Ʒ����ɫ��C�в�������ɫ����/������D����ˮ��ɫ��
��2��A�б���SO2��������������ʣ�B�б���SO2Ư���ԣ�C�б���SO2�����ԣ�D�б���SO2�� ��ԭ�ԣ���ȷ��Ϊ���ڣ��٣��ܣ��ۣ�
��3��SO2���� �� ɫ �� ��ϳɲ��ȶ�����ɫ������������ɫ�����Ⱥ������ȶ�����ɫ�����зֽ��ͷų�SO2�����ʻָ�Ϊԭ������ɫ����ȷ��Ϊ����Һ�ָ���ɫ��SO2Ư���Ծ����Ȳ��ȶ��ԣ�
��4��Br2+2H2O+SO2=2HBr+H2SO4����Һ�к���SO42-����Ba2+�� �� �� �� ɫ �� ��Ba SO4����ȷ�𰸣�������ɫ������
��5������ �� �� �� �� �� �� SO2��Ӧ �� �� �� �� �� �κ�ˮ����ȷ�𰸣�2NaOH+SO2=Na2SO3+H2O
��6���� �� ���� �������� ������ ��֤ �� �������� ȷ �� ����������ͨ�뵽��������Һ������Һ���ɫ������
���÷���ʽ��ʾΪH2S+ Cl2= 2HCl+ S��

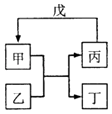
����Ŀ���ס��ҡ�������������ת����ϵ��ͼ��ʾ����Ӧ������ȥ����ͷ��ʾһ��ת���������и������У���������ͼת����ϵ���ǣ� ��
�� | �� | �� | �� | |
�� | SiO2 | NaOH | Na2SiO3 | CO2 |
�� | Fe | H2O | Fe2O3 | H2 |
�� | Al��OH��3 | NaOH��Һ | NaAlO2��Һ | ����CO2 |
�� | Na2O2 | CO2 | O2 | Na |
A.�٢�
B.�٢�
C.�ڢ�
D.�٢�