��Ŀ����
A��B��C����ǿ����ʣ�������ˮ�е����������ΪNa����Ag����NO3-��SO42-��Cl-������ͼ��ʾװ���У��ס��ҡ��������ձ����ηֱ�ʢ��������A��B��C������Һ���缫��Ϊʯī�缫����ͨ��Դ������һ��ʱ�������ձ���c�缫����������10.8�ˡ������¸��ձ�����Һ��pH����ʱ��t�Ĺ�ϵ��ͼ��ʾ���ݴ˻ش��������⣺
(1)MΪ��Դ���� ����(��д����������)���ס��������ձ��еĵ���ʷֱ�Ϊ���� ���� (��д��ѧʽ)��
(2)����缫f�����ɵ������ڱ�״�������Ϊ���� L��
(3)д�����ձ��еĵ�ⷴӦ����ʽ�� ��
(4)���������Һ�����Ϊ10L�������Һ��pHΪ�� ��
��1���� NaCl AgNO3 ��2��0.56L ��3��4AgNO3��2H2O 4Ag��4HNO3��O2�� ��4��12
4Ag��4HNO3��O2�� ��4��12
���������������1������һ��ʱ�������ձ���c�缫����������10.8�ˣ���˵��c�缫����������M�Ǹ�����N��������f��������e��������d��������b��������a�����������е���pH���ͣ�˵��������ǿ����˵��ҺӦ������������Һ������pH���ߣ�˵��������ǿ����˵��ҺӦ�����Ȼ��ơ�����pH���䣬���൱���ǵ��ˮ����˵��Һ�������ƻ������ơ�
��2��c�缫�����ĵ����������ʵ�����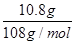 ��0.1mol��ת�Ƶ��ӵ����ʵ�����0.1mol��f�缫����������Һ�е�OH���ŵ磬4OH����4e����2H2O��O2��������ݵ���ת���غ��֪���������������ʵ�����
��0.1mol��ת�Ƶ��ӵ����ʵ�����0.1mol��f�缫����������Һ�е�OH���ŵ磬4OH����4e����2H2O��O2��������ݵ���ת���غ��֪���������������ʵ�����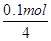 ��0.025mol����״���µ������0.025mol��22.4L/mol��0.56L��
��0.025mol����״���µ������0.025mol��22.4L/mol��0.56L��
��3�����е��������������Һ�����ⷴӦ����ʽΪ4AgNO3��2H2O 4Ag��4HNO3��O2����
4Ag��4HNO3��O2����
��4�����е�������Ȼ��ƣ����ķ���ʽΪ2NaCl��2H2O 2NaOH��H2����Cl2�������ݵ����غ��֪����Ӧ�������������Ƶ����ʵ�����0.1mol����Ũ����
2NaOH��H2����Cl2�������ݵ����غ��֪����Ӧ�������������Ƶ����ʵ�����0.1mol����Ũ����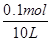 ��0.01mol/L����pH��12��
��0.01mol/L����pH��12��
���㣺������ԭ�����й��ж���Ӧ��

Ϊ��̽��ԭ��غ͵��صĹ���ԭ����ij�о���ѧϰС��ֱ�����ͼ��ʾ��װ�ý���ʵ�顣��ͼ�ش����⡣

I����ͼ����ʾװ�ý��е�һ��ʵ��ʱ��
��1���ڱ�֤�缫��Ӧ���������£��������Cu���缫���� ������ţ���
| A��ʯī | B��þ | C���� | D���� |
II����С��ͬѧ��ͼ����ʾװ�ý��еڶ���ʵ��ʱ���֣��������������������Y����Һ����Ϻ�ɫ��ֹͣʵ��۲쵽���缫���Ա�ϸ�����Һ��Ȼ���塣��������֪�����������FeO42-������Һ�г��Ϻ�ɫ�������ʵ������������Ϣ���ش��������⣺
��3���������У�X����Һ��pH ���������С�����䡱��
��4���������У�Y�������ĵ缫��ӦΪ4OH?��4e?=2H2O+O2���� ��
��5��������һ��ʱ�������X���ռ���672mL���壬Y�缫�����缫��������С0��28g������Y���ռ�������Ϊ mL����������Ϊ��״��ʱ�����������
��6��K2FeO4��ZnҲ������ɼ��Ե�أ�K2FeO4�ڵ������Ϊ�������ϣ����ط�ӦΪ��
2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2���õ�����������ĵ缫��ӦʽΪ ��





 2Ni(OH)2������������Ϣ�жϣ���϶��������»����ʱ����
2Ni(OH)2������������Ϣ�жϣ���϶��������»����ʱ����
 Cu2O��H2���������ĵ缫��Ӧʽ��_____________________��
Cu2O��H2���������ĵ缫��Ӧʽ��_____________________��