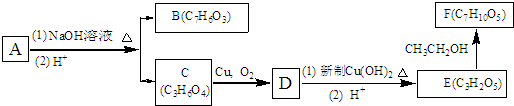
题目内容
可以用一种试剂鉴别苯、CCl4、乙醛、甲酸、乙酸、甲酸甲酯六种液态物质的是( )
| A、新制的氢氧化铜悬浊液,并加热 |
| B、Br2水 |
| C、高锰酸钾酸性溶液 |
| D、FeCl3溶液 |
考点:有机物的鉴别
专题:
分析:苯、CCl4都不溶于水,但二者密度大小不同,乙醛、甲酸、乙酸都易溶于水,其中乙醛含有-CHO,具有还原性,可用新制Cu(OH)2悬浊液检验,乙酸具有酸性,甲酸既具有酸性又具有还原性,甲酸甲酯不溶于水,加热可与氢氧化铜发生氧化还原反应,以此选择鉴别试剂.
解答:
解:A.加入新制的氢氧化铜悬浊液,苯的密度比水小,不溶于水,在上层,四氯化碳的密度比水大,在下层,乙醇不反应,乙醛在加热时生成砖红色沉淀,乙酸和氢氧化铜发生中和反应,氢氧化铜溶解,甲酸能溶解氢氧化铜,含有醛基,加热时有砖红色沉淀生成,甲酸甲酯不溶于水,加热可与氢氧化铜发生氧化还原反应,可鉴别,故A正确;
B.加入溴水,不能鉴别乙醛、甲酸,故B错误;
C.高锰酸钾具有强氧化性,不能鉴别乙醛、甲酸,故C错误;
D.FeCl3溶液不能鉴别苯、甲酸甲酯以及乙醛、甲酸、乙酸,故D错误.
故选A.
B.加入溴水,不能鉴别乙醛、甲酸,故B错误;
C.高锰酸钾具有强氧化性,不能鉴别乙醛、甲酸,故C错误;
D.FeCl3溶液不能鉴别苯、甲酸甲酯以及乙醛、甲酸、乙酸,故D错误.
故选A.
点评:本题考查有机物的鉴别,题目难度中等,本题注意把握常见有机物的性质和鉴别方法,鉴别有机物时,要有明显的现象.

练习册系列答案
相关题目
实验室有一瓶久置的白色K2SO3粉末,为确定其是否被氧化及其成分,元素分析表明粉末中K和S元素的质量比为39:16,下列结论正确的是( )
| A、根据测得的元素质量比可推测该粉末为纯净物 |
| B、将粉末溶于水,加入氯化钡,有白色沉淀生成,证明原粉末含K2SO4 |
| C、将粉末加入盐酸中,产生气泡,证明K2SO3未变质 |
| D、将粉末溶于水,加入氯化钡和过量的盐酸,有白色沉淀和气泡生成,证明原粉末是K2SO4和K2SO3的混合物 |
 从中药材提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率.已知金丝桃素的结构简式如图所示.下列有关说法正确的是( )
从中药材提取的金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率.已知金丝桃素的结构简式如图所示.下列有关说法正确的是( )| A、金丝桃素的分子式为C17H22O3N |
| B、金丝桃素不能与浓硫酸和浓硝酸的混合液反应 |
| C、金丝桃素能在NaOH溶液中加热反应得到两种芳香族化合物 |
| D、金丝桃素在一定条件下能发生加成、酯化、消去和氧化反应 |
下列各组离子能大量共存的是( )
| A、Cu2+、NO3-、Cl-、K+ |
| B、Fe3+、SO4-、SCN-、Na+ |
| C、Al3+、K+、AlO2-、Cl- |
| D、Fe2+、NO3-、Cl-、H+ |
为了鉴定溴乙烷中溴元素的存在,试分析①~⑥的各步实验,其中操作顺序合理的是( )①加入AgNO3溶液 ②加入NaOH溶液 ③加热 ④加入蒸馏水 ⑤用HNO3酸化溶液⑥加入NaOH溶液醇溶液.
| A、①②③⑤ | B、②③⑤① |
| C、⑥③⑤① | D、④②⑤③ |
 25摄氏度时,在20ml 0.1mol/L NaOH溶液中逐滴加入 0.2mol/L的醋酸溶液,曲线如图所示有关离子浓度关系的比较中,正确的是( )
25摄氏度时,在20ml 0.1mol/L NaOH溶液中逐滴加入 0.2mol/L的醋酸溶液,曲线如图所示有关离子浓度关系的比较中,正确的是( )| A、在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
| B、在A点:c(CH3COO-)+c(CH3COOH)=2c(Na+) |
| C、在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-) |
| D、在C点:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
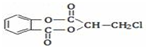 )在一定条件下可以发生如图所示的转化(其它产物和水已略去).请回答下列问题:
)在一定条件下可以发生如图所示的转化(其它产物和水已略去).请回答下列问题: