题目内容
11.将标准状况下22.4L某烃完全燃烧,生成54gH2O和44.8LCO2(标况下)(1)通过计算求出该烃的分子式
(2)写出该烃的结构式.
分析 有机物的物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,n(CO2)=$\frac{44.8L}{22.4L/mol}$=2mol,n(H2O)=$\frac{54g}{18g/mol}$=3mol,可知有机物含有2个C原子、6个H原子,分子式为C2H6,以此解答该题.
解答 解:(1)n(H2O)=$\frac{54g}{18g/mol}$=3mol,
n(H)=2n(H2O)=6mool,
n(CO2)=$\frac{44.8L}{22.4L/mol}$=2mol,
n(C)=n(CO2)=2mool,
有机物的物质的量为$\frac{22.4L}{22.4L/mol}$=1mol,
可知有机物含有2个C原子、6个H原子,分子式为C2H6,
答:该烃的分子式为C2H6;
(2)C2H6为乙烷,结构式为 ,
,
答:该烃的结构式为 .
.
点评 本题考查了有机物分子式的确定,为高频考点,侧重考查学生的分析、计算能力,题目难度中等,注意掌握质量守恒定律在确定有机物分子式中的应用.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
1.将金属A和金属B分别放入稀硫酸中有氢气生成.若将金属A和金属B相连后投入稀硫酸中发现A被氧化,B未被氧化.关于A、B的叙述正确的是( )
| A. | 金属活动性A<B | |
| B. | 还原性B>A | |
| C. | 在后者装置中金属A发生还原反应,金属B发生氧化反应 | |
| D. | 在后者装置中金属B的表面有明显气泡产生,金属A表面无明显现象 |
2. 用已知浓度的NaOH溶液测定某草酸【H2C2O4】溶液的浓度,参考图,从下表中选出正确选项( )
用已知浓度的NaOH溶液测定某草酸【H2C2O4】溶液的浓度,参考图,从下表中选出正确选项( )
 用已知浓度的NaOH溶液测定某草酸【H2C2O4】溶液的浓度,参考图,从下表中选出正确选项( )
用已知浓度的NaOH溶液测定某草酸【H2C2O4】溶液的浓度,参考图,从下表中选出正确选项( )| 锥形瓶中的溶液 | 滴定管中的溶液 | 选用指示剂 | 选用滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 酚酞 | (乙) |
| C | 碱 | 酸 | 甲基橙 | (甲) |
| D | 酸 | 碱 | 酚酞 | (甲) |
| A. | A | B. | B | C. | C | D. | D |
16.下列变化中,吸收的热量用于克服分子间作用力的是( )
| A. | 加热氯化钠晶体使之熔化 | B. | 加热碘化氢气体使之分解 | ||
| C. | 加热硅晶体使之熔化 | D. | 液氨受热蒸发 |
3.现有a、b、c、d四种金属,①a、b合金铸造的日用品暴露在潮湿空气中a先被腐蚀;②电解b、c的硫酸盐混合溶液,电极上金属c析出后再析出b;③d的硝酸盐溶液呈中性,四种金属活泼性由强到弱的顺序是( )
| A. | d、a、b、c | B. | d、b、a、c | C. | a、b、c、d | D. | a、b、d、c |
4.下列是元素周期表的前三周期中的部分元素
(1)表中所标出的元素当中,最活泼的金属元素是K,最活泼的非金属元素是F,最不活泼的元素是Ne;
(2)K和Mg两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:KOH大于Mg(OH)2 (大于/小于);
(3)Si元素位于元素周期表的第三周期第ⅣA族,它的最高价氧化物的化学式是SiO2;其最高价氧化物对应水化物的化学式为H2SiO3.
(4)已知①2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl.据此推断,活泼性比较:O2小于Cl2 (大于/小于);
另由③Cl2+2NaBr=Br2+2NaCl,可推断氧化性比较:Cl2大于 Br2 (大于/小于).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | Li | C | N | O | F | Ne | ||
| 三 | Na | Mg | S | Cl | ||||
| 四 | K | Ca | Br |
(2)K和Mg两种元素的最高价氧化物对应的水化物都是碱,则这两种碱的碱性强弱为:KOH大于Mg(OH)2 (大于/小于);
(3)Si元素位于元素周期表的第三周期第ⅣA族,它的最高价氧化物的化学式是SiO2;其最高价氧化物对应水化物的化学式为H2SiO3.
(4)已知①2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;②Cl2和H2混合,在光照下就可以发生爆炸,生成HCl.据此推断,活泼性比较:O2小于Cl2 (大于/小于);
另由③Cl2+2NaBr=Br2+2NaCl,可推断氧化性比较:Cl2大于 Br2 (大于/小于).
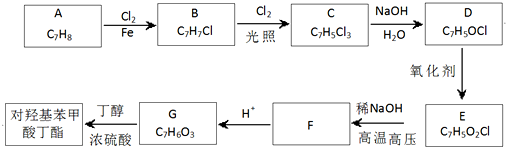
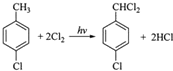 ;
; ;
; ;
;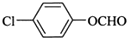 (写结构简式).
(写结构简式).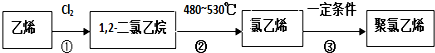
 ,反应类型为加聚反应;
,反应类型为加聚反应;
 .
. .
.