题目内容
mA(s)+nB(g)?qC(g)的可逆反应中,图甲在恒温条件达平衡时,B的体积分数(B%)与压强(p)的关系,图乙表示在一定条件下达到平衡(v正=v逆)后t1时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,有关叙述正确的是?( )

| A、n<q |
| B、n>q? |
| C、正反应为放热反应? |
| D、X点比Y点反应速率快 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由图象的曲线变化特征可知,增大压强,B的百分含量增大,说明平衡向逆反应方向移动,由于A为固体,则有n<q,在曲线上的点为平衡状态,以此来解答该题.
解答:
解:A、B.由图象的曲线变化特征可以看出,增大压强,B的百分含量增大,说明平衡向逆反应方向移动,由于A为固体,则有n<q,故A正确,B错误;
C.图象乙改变条件正逆反应速率都增大,逆反应速率增大的大多,平衡逆向进行,温度升高平衡逆向进行,正反应为放热反应,故C正确;
D.由图象可以看出X点的压强小于Y点压强,压强越大,反应速率越大,故X点比Y点的反应速率慢,故D错误.
故选:AC.
C.图象乙改变条件正逆反应速率都增大,逆反应速率增大的大多,平衡逆向进行,温度升高平衡逆向进行,正反应为放热反应,故C正确;
D.由图象可以看出X点的压强小于Y点压强,压强越大,反应速率越大,故X点比Y点的反应速率慢,故D错误.
故选:AC.
点评:本题考查化学平衡曲线问题,题目难度不大,本题注意分析纵坐标随横坐标变化的趋势,特别是曲线的上的点与曲线外的点的区别.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2007年7月2日,美、德两国成功合成出具有化学特性的氢铝化合物(AlH3)n,最简单的氢铝化合物是Al2H6,它的熔点为150℃,燃烧热极高.下列关于氢铝化合物的推测不正确的是( )
| A、氢铝化合物与水反应生成氢氧化铝和氢气 |
| B、氢铝化合物中铝显+3价,H显-1价 |
| C、氢铝化合物中不可能存在AlnH2n+2(n为正整数) |
| D、氢铝化合物燃烧生成氧化铝和水 |
电离平衡常数是衡量弱电解质电离程度强弱的物理量.已知:
在25℃条件下,下列有关说法正确的是( )
| 化学式 | 电离常数(25℃) |
| C6H5OH | K=1.1×10-10 |
| CH3COOH | K=1.74×10-5 |
| H2CO3 | K1=4.2×10-7;K2=5.6×10-11 |
| A、0.1mol/L的各溶液的pH关系为:pH(C6H5OH)>pH(Na2CO3)>pH(CH3COONa) |
| B、NaHCO3溶液中,c(OH-)=2c(H2CO3)+c(H+)+c(CO32-) |
| C、amol/L醋酸溶液与bmol/LNaOH溶液等体积混合,所得溶液中c(Na+)>c(CH3COO-),则a一定小于或等于b |
| D、向苯酚钠溶液中通入少量CO2后的溶液:c(C6H5O-)+c(C6H5OH)=c(Na+) |
某有机物的分子结构为: ,该分子中最多可以有多少个原子共平面( )
,该分子中最多可以有多少个原子共平面( )
 ,该分子中最多可以有多少个原子共平面( )
,该分子中最多可以有多少个原子共平面( )| A、18 | B、20 | C、22 | D、24 |
化学与生活密切相关.下列说法不正确的是( )
| A、乙烯可作水果的催熟剂 |
| B、甘油可用于护肤用品 |
| C、料酒可以除去食物中的腥味 |
| D、裂化汽油可用作萃取剂 |
下列应用不符合勒夏特列原理的是( )
| A、加热灼烧AlCl3溶液,最后得到氧化铝固体 |
| B、CaCO3沉淀中滴加盐酸 |
| C、硫酸工业中通常通入过量的空气 |
| D、合成氨反应中温度选择450℃左右 |
在高温下,反应2HBr(g)?H2(g)+Br2(g)(△H>0)达到平衡时,要使混合气体的颜色变浅,且使Br2的百分含量保持不变,可采取的方法是( )
| A、增大体积 |
| B、增大压强 |
| C、降低温度 |
| D、保持体积不变增加氢气 |
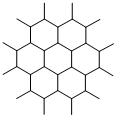 2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家.单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料.下列叙述正确是( )
2010年诺贝尔物理学奖用于表彰首次剥离出单层石墨的科学家.单层石墨称为石墨烯,这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料.下列叙述正确是( )| A、石墨烯和金刚石互为同分异构体 |
| B、石墨烯是一种有机物 |
| C、石墨烯中碳原子与共价键的个数比为1:3 |
| D、石墨烯可导电,但它不是电解质 |