题目内容
14.下列有关说法正确的是( )| A. | 在酒精灯加热条件下,Na2CO3、NaHCO3固体都能发生分解 | |
| B. | 用含硅胶、铁粉的透气小袋与食品一起密封包装 | |
| C. | H2、SO2、NH3三种气体都可用浓硫酸干燥 | |
| D. | SiO2既能和氢氧化钠溶液反应也能和氢氟酸反应,所以是两性氧化物 |
分析 A.碳酸钠稳定,受热不分解;
B.硅胶具有吸水性,铁粉具有还原性;
C.浓硫酸能够与氨气反应;
D.两性氧化物是指:既能与酸又能与碱反应,只生成盐和水的氧化物.
解答 解:A.在酒精灯加热条件下,碳酸氢钠分解,碳酸钠不分解,故A错误;
B.用含硅胶、铁粉的透气小袋与食品一起密封包装,可以防止食品受潮、氧化而变质,延长保存时间,故B正确;
C.氨气为碱性气体,能够与浓硫酸反应,不能用浓硫酸干燥,故C错误;
D.氢氟酸与二氧化硅反应生成四氟化硅和水,不符合两性氧化物的定义,不是两性氧化物,故D错误;
故选:B.
点评 本题考查了元素化合物知识,熟悉碳酸钠、碳酸氢钠、硅胶、铁粉、浓硫酸、二氧化硅的性质是解题关键,题目难度不大,注意浓硫酸不能干燥还原性气体和碱性气体,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
5.下列各项中表达正确的是( )
| A. | F-的结构示意图: | B. | 乙烯的结构简式CH2CH2 | ||
| C. | NaCl的电子式: | D. | N2的结构式::N≡N: |
2.节能减排、低碳生活已经成为时尚,下列举措不符合这一要求的是( )
| A. | 购物尽量使用可反复使用的布袋 | B. | 保持饮水机24小时开启 | ||
| C. | 尽量避免使用一次性餐具 | D. | 随手关灯 |
9.下列有关物质用途的说法中,不正确的是( )
| A. | 氢氟酸可用来刻蚀玻璃 | B. | 过氧化钠常用作供氧剂 | ||
| C. | 晶体硅可用于制作光导纤维 | D. | 漂白粉可用作游泳池的消毒剂 |
19.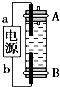 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
 某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )
某同学设计了一种利用电解法制取Fe(OH)2的实验装置(如图),通电后,溶液中产生白色沉淀,且较长时间不变色.下列说法中正确的是( )| A. | 电源中a一定为负极,b一定为正极 | |
| B. | 可以用NaCl作为电解质,但不能用Na2SO4 | |
| C. | A、B两端都必须用铁作电极 | |
| D. | 阴极上发生的反应是:2H++2e-═H2↑ |
6.一定温度下,有可逆反应:2A(g)+2B(g)?C(g)+3D(g);△H<0.现将2 mol A和2 mol B充入体积为V的甲容器,将2 mol C和6 mol D充入乙容器并使乙容器在反应开始前的体积为2V(如图1).

关于两容器中反应的说法正确的是( )

关于两容器中反应的说法正确的是( )
| A. | 甲容器中的反应先达到化学平衡状态 | |
| B. | 两容器中的反应均达平衡时,平衡混合物中各组份的体积百分组成相同,混合气体的平均相对分子质量不相同 | |
| C. | 两容器达平衡后升高相同的温度,两容器中物质D的体积分数随温度变化如图2所示 | |
| D. | 在甲容器中再充入2 mol A和2 mol B,平衡后甲中物质C的浓度是乙中物质C的浓度的2倍 |
3.下列化合物为苯的同系物的是( )


| A. | ①② | B. | ③④ | C. | ①④ | D. | ②④ |
