题目内容
欲测定某NaOH溶液的浓度,操作步骤如下:①用碱式滴定管量取25.00mL待测溶液注入锥形瓶中;
②向锥形瓶中滴入酚酞作指示剂,用0.1000mol/L标准盐酸进行滴定.滴定至终点,测得所耗盐酸的体积为V1 mL;
③重复以上过程,第二次测得所耗盐酸的体积为V2 mL.
请回答:
(1)滴定时边滴边摇动锥形瓶,眼睛应观察______,滴定终点时的现象为锥形瓶中的溶液由______.
(2)
| 滴定次数 | 待测液体积/mL | 标准盐酸体积/mL | |
| 滴定前读数/mL | 滴定后读数/mL | ||
| 第一次 | 25.00 | 0.40 | 20.38 |
| 第二次 | 25.00 | 4.00 | 24.02 |
【答案】分析:(1)眼睛应观察锥形瓶内溶液颜色的变化;滴定前酚酞显示红色,滴定结束变成无色;
(2)算出两次消耗盐酸的体积,求出待测NaOH溶液的物质的量浓度.
解答:解:(1)滴定过程中,眼睛一定看着锥形瓶内溶液颜色的变化;氢氧化钠溶液中,酚酞呈现红色,完全中和后,溶液变成了无色;
故答案为:锥形瓶内溶液颜色的变化;红色变为无色且在半分钟内不恢复;
(2)消耗盐酸体积为 V1=20.38ml-0.40ml=19.98ml;V2=24.02ml-4.00ml=20.02ml;v平均= =20.00ml
=20.00ml
c(NaOH)=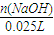 =
=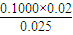 =0.0800(mol/L);
=0.0800(mol/L);
故答案为:0.0800 mol/L
点评:本题考查酸碱中和滴定,注重了滴定基础知识考查,难度中等.
(2)算出两次消耗盐酸的体积,求出待测NaOH溶液的物质的量浓度.
解答:解:(1)滴定过程中,眼睛一定看着锥形瓶内溶液颜色的变化;氢氧化钠溶液中,酚酞呈现红色,完全中和后,溶液变成了无色;
故答案为:锥形瓶内溶液颜色的变化;红色变为无色且在半分钟内不恢复;
(2)消耗盐酸体积为 V1=20.38ml-0.40ml=19.98ml;V2=24.02ml-4.00ml=20.02ml;v平均=
 =20.00ml
=20.00mlc(NaOH)=
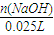 =
=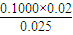 =0.0800(mol/L);
=0.0800(mol/L);故答案为:0.0800 mol/L
点评:本题考查酸碱中和滴定,注重了滴定基础知识考查,难度中等.

练习册系列答案
 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案
相关题目
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下: