题目内容
19.下列叙述中正确的是( )| A. | 1mol H2与0.5mol H2和O2的混合物所含的原子数目相同 | |
| B. | 32g O2含有6.02×1023个氧分子 | |
| C. | 1mol H2O中含有2mol H2,1mol O,总共所含电子的物质的量为10mol | |
| D. | 物质的量为1mol 的任何微粒的质量与NA个该种微粒的质量在任何情况下都相等 |
分析 A.1mol H2与0.5mol H2和O2的混合物所含的原子物质的量分别为2mol、1mol;
B.根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算;
C.水中不含氢气分子;
D.1mol微粒的数目为NA.
解答 解:A.1mol H2含有2mol H原子,0.5mol H2和O2的混合物所含的原子为1mol,二者不同,故A错误;
B.n(O2)=$\frac{32g}{32g/mol}$=1mol,含有6.02×1023个氧分子,故B正确;
C.水中不含氢气分子,故C错误;
D.1mol微粒的数目为NA,则物质的量为1mol 的任何微粒的质量与NA个该种微粒的质量在任何情况下都相等,故D正确.
故选BD.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析能力和计算能力的考查,注意把握相关计算公式的运用,难度不大.

练习册系列答案
相关题目
10.完全燃烧CO和H2的混合气体共50mL,需要同温同压下的氧气( )
| A. | 20mL | B. | 25mL | C. | 50mL | D. | 无法计算 |
14.已知键能数据:1mol H-N:390.8kJ/mol;1mol N≡N:946kJ/mol;1mol H-H:436.0kJ/mol对反应3H2+N2═2NH3,其反应热的表述正确的是( )
| A. | △H=-600.4kJ/mol | B. | △H=-1081.6kJ/mol | ||
| C. | △H=+90.8kJ/mol | D. | △H=-90.8kJ/mol |
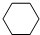 ,名称是环己烷.
,名称是环己烷.