题目内容
19.核内中子数为N的R2+离子,质量数为A,则n克它的氧化物中所含质子的物质的量是( )| A. | $\frac{n(A-N+10)}{(A+16)}$mol | B. | $\frac{n(A-N+8)}{(A+16)}$mol | C. | (A-N+2)mol | D. | n(A-N+6)mol |
分析 R2+离子对应的氧化物为RO,该氧化物的摩尔质量为(A+16)g/mol,含有质子数为:(A-N)+8,根据n=$\frac{m}{M}$计算出该氧化物的物质的量,然后计算出含有质子的物质的量.
解答 解:核内中子数为N的R2+离子,质量数为A,则R的质子数=A-N,其形成的氧化物为RO,氧化物RO的摩尔质量为(A+16)g/mol,含有质子数=A-N+8,
ng该氧化物的物质的量为:$\frac{ng}{(A+16)g/mol}$=$\frac{n}{A+16}$mol,含有的质子的物质的量为:$\frac{n}{A+16}$mol×(A-N+8)=$\frac{n(A-N+8)}{A+16}$mol,
故选B.
点评 本题考查了物质的量的计算,题目难度不大,明确质量数与质子数、中子数的关系为解答关键,注意掌握相对分子质量与摩尔质量的关系,试题有利于学生的分析能力及化学计算能力.

练习册系列答案
相关题目
10.在反应中,既能放出气体,又不是氧化还原反应的是( )
| A. | Na和水反应 | B. | Na2O2和水反应 | ||
| C. | 氯化铵与氢氧化钙反应 | D. | MnO2与浓盐酸共热 |
7.国际互联网上报道:目前世界上有近20亿人患有缺铁性贫血.这里的“铁”是指( )
| A. | 铁单质 | B. | +2价铁元素 | C. | +3价铁元素 | D. | 三氧化二铁 |
4.下列化学用语表达不正确的是( )
| A. | HCl的结构式为:H-Cl | B. | 水分子的结构式为: | ||
| C. | S2-的离子结构示意图为: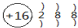 | D. | N2的电子式为: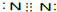 |
11.下列仪器,能加热但应该垫石棉网使用的是( )
| A. | 蒸发皿 | B. | 锥形瓶 | C. | 坩埚 | D. | 容量瓶 |
1.下列有关反应的能量变化,错误的是( )
| A. | 化学反应中,有放热反应也有吸热反应 | |
| B. | 化学反应中的能量变化主要由化学键的变化引起的 | |
| C. | 吸热反应一定要加热才能发生 | |
| D. | 盐酸与NaOH溶液的反应是放热反应 |
 含同一元素的常见物质A、B、C,有如下转化关系(条件未标注):
含同一元素的常见物质A、B、C,有如下转化关系(条件未标注):