题目内容
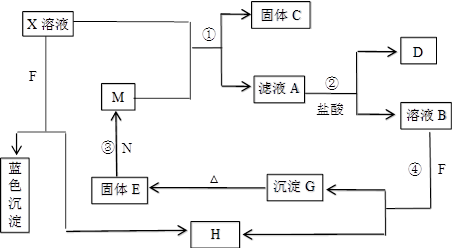
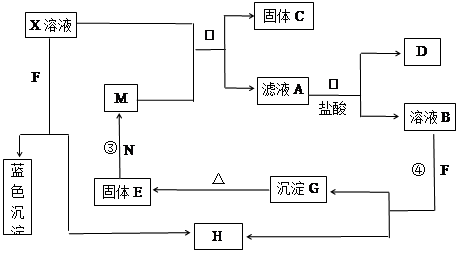
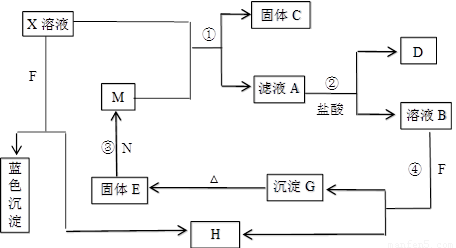
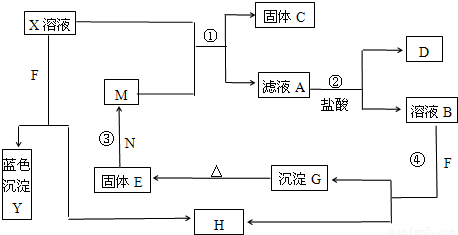
已知A为中学化学中常见的金属,而X、Y为中学化学中常见的非金属单质.C、X、E、F、G常温下为气体,J为无色液体,B是一种盐,受热易分解,现用A和石墨作电极,B的浓溶液作电解质溶液形成原电池物质之间的转化关系如图所示(其中部分反应的条件和生成物已被省略)
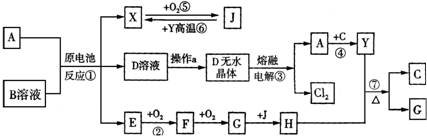
上图中H的浓溶液与炽热的Y单质发生反应⑦,生成C、G的同时也生成了J.请根据图示回答下列问题:
(1)金属A为 ,操作a是将D溶液与HCl的气流中蒸干,HCl所起的作用是 .
(2)写出E的电子式 ,该分子的空间构型 ,C的结构式 .
(3)写出反应⑦的化学方程式 .
(4)原电池①的总反应为 .
(5)写出反应②的化学方程式 .

上图中H的浓溶液与炽热的Y单质发生反应⑦,生成C、G的同时也生成了J.请根据图示回答下列问题:
(1)金属A为
(2)写出E的电子式
(3)写出反应⑦的化学方程式
(4)原电池①的总反应为
(5)写出反应②的化学方程式
分析:J为液体,由转化关系X
J可知,J为H2O,X含有H元素,X为常见非金属,故X为H2;
由D无水晶体
A+Cl2,可知D为氯化物且是离子化合物,结合A+B溶液
X+D+E,可知B为氯化物,且B是一种盐,受热极易分解,反应生成的H2与E气体,B应水解呈酸性,结合E
F
G,考虑反应①是金属与NH4Cl溶液发生的原电池反应,则B为NH4Cl,E为NH3,F为NO,G为NO2,由G
H,可知H为HNO3;
Y为常见非金属,A(金属)→Y,Y+HNO3
NO2,考虑Mg与CO2反应生成碳,碳与浓硝酸反应可以生成NO2,碳与水反应可以是氢气,符合转化关系,故A为Mg,Y为碳,D为MgCl2,结合对应物质的性质以及题目要求解答该题.
| O2 |
由D无水晶体
| 电解 |
| 原电池反应 |
| O2 |
| O2 |
| H2O |
Y为常见非金属,A(金属)→Y,Y+HNO3
| △ |
解答:解:J为液体,由转化关系X
J可知,J为H2O,X含有H元素,X为常见非金属,故X为H2;
由D无水晶体
A+Cl2,可知D为氯化物且是离子化合物,结合A+B溶液
X+D+E,可知B为氯化物,且B是一种盐,受热极易分解,反应生成的H2与E气体,B应水解呈酸性,结合E
F
G,考虑反应①是金属与NH4Cl溶液发生的原电池反应,则B为NH4Cl,E为NH3,F为NO,G为NO2,由G
H,可知H为HNO3;
Y为常见非金属,A(金属)→Y,Y+HNO3
NO2,考虑Mg与CO2反应生成碳,碳与浓硝酸反应可以生成NO2,碳与水反应可以是氢气,符合转化关系,故A为Mg,Y为碳,D为MgCl2,
(1)由以上分析可知A为Mg,D为MgCl2,溶液水解呈酸性,为抑制水解,应在HCl气流中,
故答案为:Mg;抑制Mg2+水解,带出水蒸气;
(2)E为NH3,电子式为 ,为三角锥形分子,C为CO2,为直线形分子,结构式为O=C=O,故答案为:
,为三角锥形分子,C为CO2,为直线形分子,结构式为O=C=O,故答案为: ;三角锥形;O=C=O;
;三角锥形;O=C=O;
(3)反应⑦为浓硝酸与碳的反应,方程式为C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O;
(4)原电池①生成氯化镁、氢气和氨气,则总反应为Mg+2NH4Cl
MgCl2+NH3↑+H2↑,故答案为:Mg+2NH4Cl
MgCl2+NH3↑+H2↑;
(5)反应②为氨气的催化氧化,反应的方程式为4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O.
| O2 |
由D无水晶体
| 电解 |
| 原电池反应 |
| O2 |
| O2 |
| H2O |
Y为常见非金属,A(金属)→Y,Y+HNO3
| △ |
(1)由以上分析可知A为Mg,D为MgCl2,溶液水解呈酸性,为抑制水解,应在HCl气流中,
故答案为:Mg;抑制Mg2+水解,带出水蒸气;
(2)E为NH3,电子式为
 ,为三角锥形分子,C为CO2,为直线形分子,结构式为O=C=O,故答案为:
,为三角锥形分子,C为CO2,为直线形分子,结构式为O=C=O,故答案为: ;三角锥形;O=C=O;
;三角锥形;O=C=O;(3)反应⑦为浓硝酸与碳的反应,方程式为C+4HNO3(浓)
| ||
| ||
(4)原电池①生成氯化镁、氢气和氨气,则总反应为Mg+2NH4Cl
| ||
| ||
(5)反应②为氨气的催化氧化,反应的方程式为4NH3+5O2
| ||
| 高温高压 |
| ||
| 高温高压 |
点评:本题考查无机物的推断,为高考常见题型和高频考点,侧重于学生的分析能力和元素化合物知识的综合运用的考查,注意把握题给信息,结合转化关系进行推断,把握给提的推断的突破口,难度中等.

练习册系列答案
相关题目