题目内容
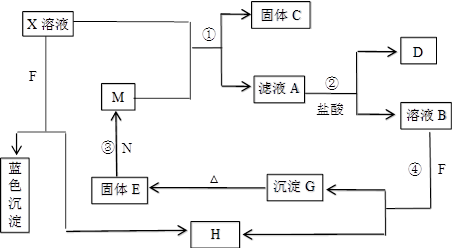
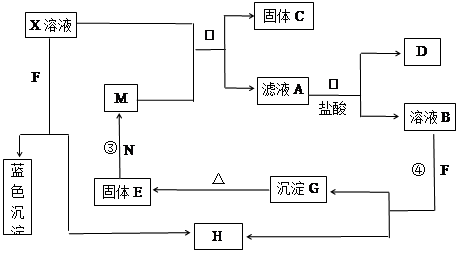
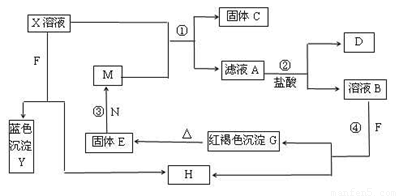
(8分)已知X为中学化学中的一种常见的盐,F为淡黄色固体;M、N为常见的金属,N的组成元素的离子半径是第三周期元素中离子半径最小的。N的最高价氧化物是耐火材料,它的晶体硬度很大,常做手表的轴承;H为气体单质,D为无色气体,在空气中会出现红棕色。各物质的转化关系如下图(部分反应产物已略去)。
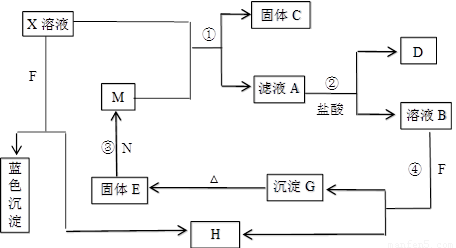
请回答下列问题:
(1)X的化学式为 ;F的电子式为 。
(2)反应②的离子方程式为_______________________________________________。
反应③的化学方程式为_______________________________________________。
(3)若向100 mL 盐X的溶液中加入10 g金属单质M的粉末,充分搅拌后,过滤,烘干
得10.16g固体C。则滤液A中溶质的物质的量浓度为________________________。(假设体积不变)
(1)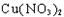 ,
,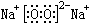 (1分/个,共2分)
(1分/个,共2分)
(2)① 3Fe2+ + NO3-+ 4H+ == 3Fe3+ + NO↑+ 2H2O(2分)
② 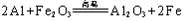 (2分)
(2分)
(3)0.2 mol/L(2分)
【解析】本题属于无机框图题,思维容量大,综合性强。这种类型恶试题关键是找准题眼,寻求突破点。根据题意可知F是过氧化钠,N是Al,D是NO。过氧化钠溶于水生成氧气,则H是氧气。蓝色沉淀是氢氧化铜,则X中含有铜离子。M和X可发生置换反应生成固体C,则C是铜,因此M是铁。反应中生成NO,说明是氧化还原反应,所以A是硝酸亚铁,B中含有铁离子,和过氧化钠反应生成氢氧化铁,氢氧化铁分解生成氧化铁,氧化铁和铝发生铝热反应即得到铁单质。硝酸铜和铁反应的方程式为Cu(NO3)2+Fe=Cu+Fe(NO3)2,每消耗1mol硝酸铜,固体质量增加8g。实际增加的质量是0.16g,则消耗的硝酸铜为 ,所以浓度是0.2mol/L。
,所以浓度是0.2mol/L。