题目内容
将一定量的CH4、O2和Na2O2放入一密封容器中,用电火花不断引燃混合气体,使其充分反应,反应结束后,容器内气体的压强趋于零(固体物质的蒸发不计,温度为150℃),其残余物质溶于水无气体放出,试求参加反应的CH4、O2和Na2O2的化学计量数之比.
答案:2∶1∶6
提示:
提示:
|
小结点评:守恒法应用于解循环反应的计算题优点是能快速推出总反应,然后可根据总反应进行有关计算,但要求明确反应物或生成物各是什么,以及部分物质的化学计量数比值. |

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
(12分)欲探究某矿石可能是由FeCO3、SiO2、Al2O3中的一种或几种组成,探究过程如下图所示。已知:碳酸不能溶解Al(OH)3沉淀。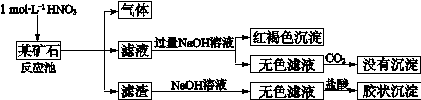
(1)Si在周期表中的位置是 。
(2)下列说法正确的是 。
| a.酸性:H2CO3>H2SiO3 | b.原子半径:O<C<Si<Al |
| c.稳定性:H2O>CH4>SiH4 | d.离子半径:O2-<Al3+ |
(4)该矿石和1 mol L-1HNO3反应的离子方程式 。
(5)工业上依据上述实验原理处理该矿石,将反应池逸出的气体与一定量的O2混合循环通入反应池中,目的是 ;若处理该矿石2.36×103 kg,得到滤渣1.2×103 kg,理论上至少需要1 mol L-1 HNO3的体积为 L。

