题目内容
15.下列说法中正确的是( )| A. | 煤的气化和液化是物理变化 | |
| B. | 煤干馏可以得到甲烷、苯和氨等重要化工原料 | |
| C. | 溴苯中混有溴,加入KI溶液,振荡,用汽油萃取出溴 | |
| D. | 苯中含苯酚杂质,可用过量浓溴水,将苯酚转化为2,4,6-三溴苯酚沉淀,过滤除去 |
分析 A.煤的气化和液化是化学变化;
B.根据煤干馏是在隔绝空气条件下对煤加强热使煤分解,可得到多种物质;
C.溴苯中混有溴,加入KI溶液,振荡,生成碘,碘易溶于溴苯;
D.苯和三溴苯酚沉淀互溶.
解答 解:A.煤的气化是让煤在高温条件下与水蒸气反应生成氢气和一氧化碳;煤的液化是利用煤制取甲醇的反应,故均为化学变化,故A错误;
B.煤干馏是在隔绝空气条件下对煤加强热使煤分解,可以得到甲烷、苯和氨等重要化工原料,故B正确;
C.溴苯中混有溴,加入KI溶液,振荡,生成碘,碘易溶于溴苯,引入新杂质,应选NaOH、分液来分离,故C错误;
D.苯酚中加入浓溴水振荡生成三溴苯酚沉淀,而苯和三溴苯酚沉淀互溶,不能用此法除去苯酚,应用NaOH溶液除去,故D错误;
故选B.
点评 本题主要考查有机物的一些基本概念和性质,以及典型的苯与苯酚中的除杂方法,属概念识记知识,平时需加强这方面知识的积累和记忆,题目难度不大.

练习册系列答案
相关题目
3.减少工业和生活废弃物的排放并合理开发利用,近年来受到了人们的普遍关注.
I.利用工业废水中的CO2制取甲醇,反应为CO2+3H2$\stackrel{催化剂}{?}$CH3OH+H2O.
(1)已知下列反应的能量变化如图1所示:
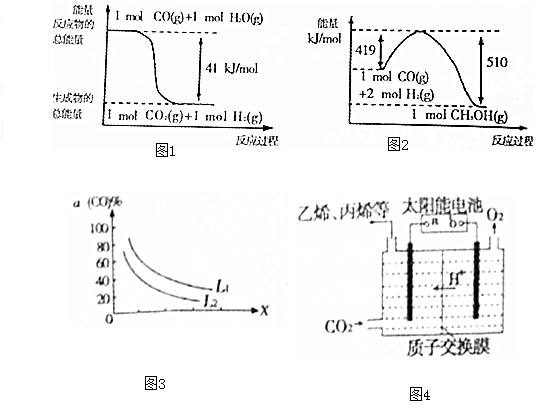
由二氧化碳和氢气制备甲醇的热化学方程式为CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-50kJ/mol.
II.利用工业废气CO合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g).
(2)一定条件下,在1L密闭容器中充入0.6mol CO和1.4mol H2,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为0.075mol/(L•min).
(3)若反应原料是来自煤的气化,已知该反应的平衡常数表达式为K=$\frac{c({H}_{2})•c(CO)}{c({H}_{2}O)}$,每生成1molH2需要吸收131.3kJ的热量.写出该反应的热化学方程式C(s)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol.
(4)t℃时,能发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g).已知反应平衡常数为400,此温度下,在1L密闭容器中加入-定量的甲醇,反应到某时刻测得各组分的物质的量浓度如表:
此刻正、逆反应速率的关系是:v(正)>v(逆)(填“>”“<”或“=”),平衡时c(CH3OCH3)的物质的量浓度是1.2mol/L.
(5)已知反应 3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图2所示.图中X表示温度(填“温度”或“压强”),判断的理由是图中表明随着X增大,CO的平衡转化率减小;如果X表示压强,压强增大,平衡向正反应方向移动,CO的平衡转化率增大,不符合条件;如果X表示温度,温度升高,平衡向逆反应方向移动,CO的平衡转化率减小,符合条件..
(6)强酸性电解质溶液中,用惰性电极电解CO2可转化为多种燃料,其原理如图3所示.b为电源的正极.电解时,生成乙烯的电极反应式为2CO2+12H++12e-=C2H4+4H2O.
I.利用工业废水中的CO2制取甲醇,反应为CO2+3H2$\stackrel{催化剂}{?}$CH3OH+H2O.
(1)已知下列反应的能量变化如图1所示:

由二氧化碳和氢气制备甲醇的热化学方程式为CO2(g)+3H2(g)=CH3OH(g)+H2O(g)△H=-50kJ/mol.
II.利用工业废气CO合成甲醇,反应为CO(g)+2H2(g)?CH3OH(g).
(2)一定条件下,在1L密闭容器中充入0.6mol CO和1.4mol H2,8min后达到平衡,CO的转化率为50%,则8min内H2的平均反应速率为0.075mol/(L•min).
(3)若反应原料是来自煤的气化,已知该反应的平衡常数表达式为K=$\frac{c({H}_{2})•c(CO)}{c({H}_{2}O)}$,每生成1molH2需要吸收131.3kJ的热量.写出该反应的热化学方程式C(s)+H2O(g)=H2(g)+CO(g)△H=+131.3kJ/mol.
(4)t℃时,能发生如下反应:2CH3OH(g)?CH3OCH3(g)+H2O(g).已知反应平衡常数为400,此温度下,在1L密闭容器中加入-定量的甲醇,反应到某时刻测得各组分的物质的量浓度如表:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol•L-1) | 0.46 | 1.0 | 1.0 |
(5)已知反应 3CO(g)+3H2(g)?CH3OCH3(g)+CO2(g),CO的平衡转化率a(CO)与温度、压强的关系如图2所示.图中X表示温度(填“温度”或“压强”),判断的理由是图中表明随着X增大,CO的平衡转化率减小;如果X表示压强,压强增大,平衡向正反应方向移动,CO的平衡转化率增大,不符合条件;如果X表示温度,温度升高,平衡向逆反应方向移动,CO的平衡转化率减小,符合条件..
(6)强酸性电解质溶液中,用惰性电极电解CO2可转化为多种燃料,其原理如图3所示.b为电源的正极.电解时,生成乙烯的电极反应式为2CO2+12H++12e-=C2H4+4H2O.
10.将9g铜和铁的混合物投入100mL稀硝酸中,充分反应后得到标准状况下1.12LNO,剩余4.8g金属;继续加入100mL等浓度的稀硝酸,金属完全溶解,又得到标准状况下1.12LNO.若向反应后的溶液中加入KSCN溶液,溶液不变红,则下列说法正确的是( )
| A. | 原混合物中铜和铁各0.065mol | |
| B. | 稀硝酸的物质的量浓度为4.0mol•L-1 | |
| C. | 第一次剩余的4.8g金属为铜和铁 | |
| D. | 向反应后的溶液中再加入该稀硝酸100mL,又得到NO在标准状况下的体积为0.56 L |
20.下列图示与对应的叙述相符的是( )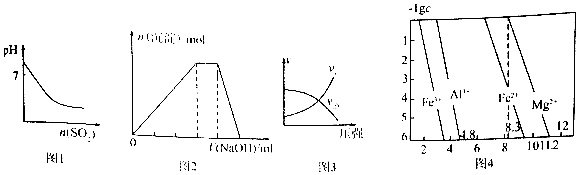

| A. | 图1表示常温下,将SO2气体通入溴水中,所得溶液pH的变化 | |
| B. | 图2表示向NH4A1(SO4)2溶液中逐滴滴入NaOH溶液,沉淀总物质的量(n)随NaOH溶液体积(V)的变化 | |
| C. | 图3表示T°C时,对于可逆反应:A(g)+B(g)?2C(g)+D(g)△H>0,正、逆反应速率与压强的关系 | |
| D. | 图4表示常温下,几种难溶氢氧化物的饱和溶液中金属离子浓度的负对数与溶液PH的关系,则在pH=7的溶液中,Fe3+、A13+、Fe2+能大量共存 |
7.某链状烃与苯互为同分异构体,其官能团只有碳碳叁键,则该烃的结构可能有( )
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
2.某温度下,在一恒容密闭容器中进行可逆反应:X(g)+Y(g)?2Z(g)+W(s)(吸热反应) 下列叙述正确的是( )
| A. | 平衡后加入少量W,逆反应速率增大 | |
| B. | 平衡后升温,只有吸热反应速率加快 | |
| C. | 当容器中混合气体的压强不再变化时,反应达到平衡 | |
| D. | 平衡后加入W,平衡未被破坏 |
 H溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是
H溶液,当金属离子全部沉淀时,得到2.54g沉淀。下列说法不正确的是 3N2,转移的电子数为NA
3N2,转移的电子数为NA 子数为2NA
子数为2NA