题目内容
某温度下,N2O4(g)?2NO2(g);△H>0.在密闭容器中达到平衡,下列说法不正确的是( )
| A、加压时(减小体积),将使正、逆反应速率增大,平衡向逆反应方向移动 |
| B、保持体积不变,加入少许NO2,将使正反应速率减小,逆反应速率增大,平衡向逆反应方向移动 |
| C、保持体积不变,加入少许N2O4,再达到平衡时,颜色变深 |
| D、保持体积不变,升高温度,再达平衡时颜色变深 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:由热化学方程式可知该反应吸热,升高温度平衡向正反应方向移动,反应物和生成物都只有一种,从平衡移动的角度分析化学平衡移动,增大浓度、压强、升温可以增大反应速率.
解答:
解:A.增大越强,反应速率增大,故A正确;
B.保持体积不变,加入少许NO2,瞬时,逆反应速率增大,正反应速率不变,然后逐渐变大,故B错误;
C.保持体积不变,加入少许N2O4,生成物的浓度增大,颜色加深,故C正确;
D.正反应吸热,升高温度平衡向正反应方向移动,颜色加深,故D正确.
故选B.
B.保持体积不变,加入少许NO2,瞬时,逆反应速率增大,正反应速率不变,然后逐渐变大,故B错误;
C.保持体积不变,加入少许N2O4,生成物的浓度增大,颜色加深,故C正确;
D.正反应吸热,升高温度平衡向正反应方向移动,颜色加深,故D正确.
故选B.
点评:本题考查化学平衡的移动问题,题目难度中等,注意方程式的特征,把握影响化学平衡移动的因素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下图是某些实验的部分装置,其中所注明的实验能达到实验目的是( )
A、 除去CO气体中的CO2气体 |
B、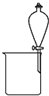 分离碘酒中的碘和酒精 |
C、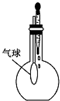 验证NH3的溶解性 |
D、 比较Na2CO3、NaHCO3的热稳定性 |
金属晶体、离子晶体、分子晶体和原子晶体的根本区别是( )
| A、基本构成微粒和微粒间的作用力不同 |
| B、外部形状不同 |
| C、金属晶体和原子晶体属于单质,分子晶体和离子晶体属于化合物 |
| D、基本构成微粒做周期性重复排列所遵循的规律不同 |
酸雨形成的主要原因是( )
| A、森林乱伐,破坏生态平衡 |
| B、工业上大量含S燃料燃烧 |
| C、制H2SO4厂排出大量尾气 |
| D、汽车尾气的排放 |
化学与人类生活、社会可持续发展密切相关,下列措施有利于节能减排、保护环境的是:
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤推广使用节能环保材料;
⑥2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)
其中符合“化学反应的绿色化”的要求的是( )
①加快化石燃料的开采与使用;
②研发易降解的生物农药;
③应用高效洁净的能源转换技术;
④田间焚烧秸秆;
⑤推广使用节能环保材料;
⑥2M+N=2P+2Q,2P+M=Q(M、N为原料,Q为期望产品)
其中符合“化学反应的绿色化”的要求的是( )
| A、①③④⑤ | B、②③⑤⑥ |
| C、①②③④ | D、②④⑤⑥ |
我们生活在五彩缤纷的世界里,以下色彩是由化学变化呈现出来的是( )
| A、雨后彩虹 | B、彩色图画 |
| C、节日焰火 | D、铜绿 |
在无色透明溶液中,不能大量共存的离子组是( )
| A、Cu2+、Na+、OH-、Cl- |
| B、K+、Na+、OH-、NO3- |
| C、OH-、NO3--、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
 用如图表示的一些物质或概念间的从属关系中不正确的是( )
用如图表示的一些物质或概念间的从属关系中不正确的是( )