题目内容
【题目】四种短周期元素在周期表中的位置如右图,其中只有M为金属元素。下列说法不正确的是( )
![]()
A. 原子半径Z<M
B. Y的最高价氧化物对应水化物的酸性比X 的弱
C. X 的最简单气态氢化物的热稳定性比Z的小
D. Z位于元索周期表中第2 周期,第ⅥA族
【答案】B
【解析】试题分析:根据元素在周期表中的位置可知,这Y、Z处于第二周期,M、X处于第三周期,只有M为金属元素,掌握M为Al元素,则X为Si元素、Y为氮元素、Z为氧元素。A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径O<Al,故A正确;B.非金属性N>Si,故酸性HNO3>H2SiO3,故B错误;C.非金属性Si<O,故氢化物稳定性SiH4<H2O,故C正确;D.Z为氧元素,位于元素周期表中第2周期第ⅥA族,故D正确;故选B。

 一线名师权威作业本系列答案
一线名师权威作业本系列答案【题目】已知Ca(OH)2、CaCO3和Ca(HCO3)2都是电解质,进行如图所示的实验,请将实验现象填入下表中的空格处。
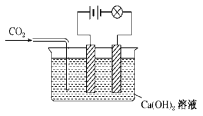
实验操作 | 灯泡亮度变化 |
(1)通入CO2之前 | 亮 |
(2)开始通入CO2时 | |
(3)恰好完全沉淀 | |
(4)沉淀完全后,继续通入过量CO2 | |
(5)再通入CO2 |
【题目】如表是元素周期表的一部分,针对表中的①~⑩元素,回答下列问题:
族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA |
一 | ① | ||||||
二 | ② | ③ | ④ | ||||
三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)在这些元素中,非金属性最强的元素符号是 ;
(2)⑧元素的氢化物的化学式为 ;
(3)金属性最活泼的元素的原子结构示意图为 ;
(4)能用来雕刻玻璃的氢化物的化学式是 ;
(5)④、⑨、⑩三种元素的原子半径由大到小的排列顺序为 (用元素符号表示);
(6)写出③元素的气态氢化物和⑨元素的最高价氧化物对应水化物相互反应的化学方程式 ;
(7)在⑤、⑥、⑦三种元素中,最高价氧化物对应的水化物的碱性最强的是 (用化学式表示);
(8)能证明元素⑩比元素⑨的非金属性强的事实是 (填序号).
A.常温下⑩单质的密度小于⑨单质的密度
B.⑩元素的气态氢化物比⑨元素的气态氢化物更稳定
C.⑩单质与氢气反应的程度比⑨单质与氢气反应的程度更剧烈
D.⑨元素的最高价氧化物对应的水化物酸性强于⑩元素的最高价氧化物对应的水化物.