题目内容
下列有关说法正确的是
A.铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连
B.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C.一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H<0
D.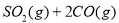

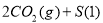 达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高
达到平衡,保持其他条件不变,分离出硫,正反应速率加快,SO2的转化率提高
AC
【解析】
试题分析:A、铁表面镀铜时,铜与电源的正极相连,作阳极,铁与电源的负极相连,作阴极,正确;B、盐酸为强酸,醋酸为弱酸,pH均为2的盐酸和醋酸,醋酸物质的量浓度大,用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积小,错误;C、该反应△S<0,能自发进行只有△H<0,正确;D、硫为液体,分离出硫,正反应速率不变,平衡不移动,SO2的转化率不变,错误。
考点:考查化学反应原理综合应用。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案(16分)Fe2+和I-是两种常见的还原性离子。
(1)向FeSO4溶液中滴加氯水,溶液由浅绿色变成黄色,反应的离子方程式为 ;向KI溶液中滴加氯水,溶液由无色变成黄色,反应的离子方程式: 。
(2)请以FeSO4溶液、KI溶液、氯水为试剂验证I-的还原性强于Fe2+。设计实验方案,补充完成实验步骤、预期现象和结论。其他限选试剂:3 mol·L-1 H2SO4、0.01 mol·L-1 KMnO4、20% KSCN、3%H2O2、淀粉溶液、紫色石蕊溶液。
实验步骤 | 预期现象与结论 |
步骤1:取2mLFeSO4溶液和2mLKI溶液混合于试管中,再滴加1~2滴氯水。 |
; |
步骤2: ____________________________________ ____________________________________。 |
|
(3)利用(2)提供的试剂证明碘与铁的化合物中铁显+2价,实验操作和现象是:
取少量样品溶于水, 。

 物质
物质 CO(g) + 3H2(g) △H=+206.0kJ·mol-1
CO(g) + 3H2(g) △H=+206.0kJ·mol-1
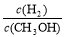 减小
减小
 乙
乙