题目内容
在下列叙述中,能说明盐酸是强酸,醋酸是弱酸的是( )
| A、将pH=4的盐酸和醋酸稀释成pH=5的溶液,盐酸加水后体积为原溶液的10倍,醋酸所需加入的水量比前者多 |
| B、盐酸和醋酸都可用相应的钠盐与浓硫酸反应制取 |
| C、相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH变大 |
| D、pH值相同的盐酸和醋酸分别跟锌反应时,产生氢气的起始速率相等 |
考点:弱电解质的判断
专题:
分析:A.依据强酸与弱酸稀释过程pH变化规律解答;
B.浓硫酸与氯化钠反应生成氯化氢,体现氯化氢易挥发性,醋酸钠与强酸反应体现醋酸的弱酸性;
C.在醋酸的溶液中存在着CH3COOH?CH3COO-+H+的电离平衡;强酸中不存在电离平衡;
D.锌与氢离子反应生成氢气的速率与氢离子的浓度有关.
B.浓硫酸与氯化钠反应生成氯化氢,体现氯化氢易挥发性,醋酸钠与强酸反应体现醋酸的弱酸性;
C.在醋酸的溶液中存在着CH3COOH?CH3COO-+H+的电离平衡;强酸中不存在电离平衡;
D.锌与氢离子反应生成氢气的速率与氢离子的浓度有关.
解答:
解:A.强酸加水后体积为原溶液的10倍,pH值变化1个单位;弱酸加水后体积为原溶液的10倍,pH变化大于1个单位,所以A能够证明盐酸为强酸,醋酸为弱酸,故A选;
B.浓硫酸与氯化钠反应生成氯化氢,体现氯化氢易挥发性,不能体现盐酸为强酸,醋酸钠与强酸反应体现醋酸的弱酸性,故B不选;
C.在醋酸的溶液中存在着CH3COOH?CH3COO-+H+的电离平衡;强酸中不存在电离平衡,所以相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH变大,故C选;
D.pH相等的醋酸和盐酸中氢离子浓度相等,所以反应开始速率相等,与电解质强弱无关,所以不能证明醋酸是弱酸、盐酸是强酸,故D不选;
故选:AC.
B.浓硫酸与氯化钠反应生成氯化氢,体现氯化氢易挥发性,不能体现盐酸为强酸,醋酸钠与强酸反应体现醋酸的弱酸性,故B不选;
C.在醋酸的溶液中存在着CH3COOH?CH3COO-+H+的电离平衡;强酸中不存在电离平衡,所以相同pH的盐酸和醋酸溶液中分别加入相应的钠盐固体,醋酸的pH变大,故C选;
D.pH相等的醋酸和盐酸中氢离子浓度相等,所以反应开始速率相等,与电解质强弱无关,所以不能证明醋酸是弱酸、盐酸是强酸,故D不选;
故选:AC.
点评:本题考查强电解质与弱电解质的定义,明确强弱电解质本质“电离程度”是解题关键,题目难度中等.

练习册系列答案
相关题目
下列有关物质的性质和应用对应正确的是( )
| A、炭在常温下化学性质不活泼,因此在埋木桩前,可将埋入地下的一段表面用火微微烧焦 |
| B、碳酸钠的水溶液呈碱性,医学上能用于治疗胃酸过多 |
| C、盐酸与苛性钠可自发进行反应,该反应可以设计成原电池 |
| D、次氯酸具有强氧化性,可以起到除去水中悬浮的杂质和杀菌消毒作用 |
一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料电池的说法中正确的是( )
| A、在熔融电解质中O2-由负极移向正极 |
| B、电池的总反应是2C4H10+13O2═8CO2+10H2O |
| C、通入空气的一极是正极,电极反应为:O2+4e-+2H2O═4OH- |
| D、通入丁烷的一极是正极,电极反应为:C4H10-26e-+13O2-═4CO2+5H2O |
金丝桃素对人工感染的H5N1亚型禽流感家禽活体具有良好的治愈率,已知金丝桃素的结构简式如图所示,与下列某试剂充分反应,所得有机物分子的官能团种类减少,则该试剂是( )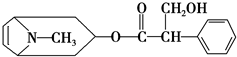

| A、Br2的CCl4溶液 |
| B、稀硫酸 |
| C、O2/Cu |
| D、H2 |
某无色溶液能与Al反应产生H2,该溶液中可能大量共存的离子组是( )
| A、K+、Na+、MnO4-、NO3- |
| B、NH4+、Mg2+、K+、NO3- |
| C、Al3+、Ba2+ HCO3-、NO3- |
| D、Ba2+、K+、CH3COO-、Cl- |
如图甲中电极a、b都是惰性电极,电解池中为2L浓度为0.5mol?L-1的CuSO4 溶液,电路中通过1mol电子后,对换电路的正负极,电路中又通过2mol电子,图乙是根据上述电解池在的a、b电极的质量(△m)、溶液pH随时间(t)的变化关系:下列有关说法正确的是( )


| A、Ⅰ代表电极a的质量变化 |
| B、Ⅱ代电极b的质量变化 |
| C、Ⅲ代表溶液pH的大小变化 |
| D、虚线Ⅳ代表0.5 mol?L-1 的CuSO4 溶液的pH,其数值为7 |
已知反应 ①稀溶液中,H+(aq)+OH-(aq)=H2O(1)△H=-57.3kJ/mol,
②2C(s)+O2(g)=2CO(g)△H=-221kJ/mol下列结论正确的是( )
②2C(s)+O2(g)=2CO(g)△H=-221kJ/mol下列结论正确的是( )
| A、碳的燃烧热为110.5kJ/mol |
| B、2molC(s)+1molO2(g)的能量比2molCO(g)的能量高221kJ |
| C、0.5 molH2SO4(浓)与1 molNaOH溶液混合,产生57.3kJ热量 |
| D、稀醋酸与稀NaOH溶液反应生成1 mol水,放出57.3kJ热量 |
某物质灼烧时,火焰颜色为黄色,下列判断正确的是( )
| A、该物质是金属钠 |
| B、该物质一定含钠元素 |
| C、该物质是钠的化合物 |
| D、该物质一定含钾元素 |