题目内容
9.工业制硫酸中的一步重要反应是SO2在400~500℃下的催化氧化:2SO2+O2?2SO3,这是一步正反应放热的可逆反应.如果反应在密闭容器中进行,下列有关说法中错误的是( )| A. | 使用催化剂是为了加快反应速率,提高生产效率 | |
| B. | 在上述条件下,SO2不可能100%地转化为SO3 | |
| C. | 为了提高SO2的转化率,应适当提高O2的浓度 | |
| D. | 达到平衡时,SO2的浓度与SO3的浓度相等 |
分析 A.催化剂可加快反应速率;
B.为可逆反应;
C.提高O2的浓度,可促进二氧化硫的转化,平衡正向移动;
D.平衡时,物质的量浓度不变.
解答 解:A.催化剂可加快反应速率,生产时间缩短,则提高生产效率,故A正确;
B.为可逆反应,则SO2不可能100%地转化为SO3,故B正确;
C.提高O2的浓度,可促进二氧化硫的转化,平衡正向移动,则可提高SO2的转化率,故C正确;
D.平衡时,物质的量浓度不变,浓度是否相等,与起始量、转化率有关,故D错误;
故选D.
点评 本题考查化学平衡,为高频考点,把握平衡与速率的影响因素、平衡移动、平衡特征为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点,题目难度不大.

练习册系列答案
相关题目
19.NA为阿伏加德罗常数,下列关于0.2mol/L K2SO4溶液的正确说法是( )
| A. | 500mL溶液中所含K+、SO42-总数为0.1NA | |
| B. | 500mL溶液中含有0.1NA个K+离子 | |
| C. | 1L溶液中K+离子浓度是0.2mol/L | |
| D. | 2L溶液中SO42-离子浓度是0.2mol/L |
20.X、Y、Z、W为四种短周期元素,它们在周期表中的位置关系如图所示.Z元素的最外层电子数等于其电子层数.下列说法中正确的是( )
| X | |||
| Z | W | Y |
| A. | Y的气态氢化物比X的氢化物沸点低 | |
| B. | Z元素的氧化物属于碱性氧化物 | |
| C. | 原子半径由小到大的顺序为:X<Z<Y<W | |
| D. | Y元素最高价氧化物对应的水化物化学式为H3YO4 |
17.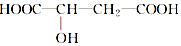 苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等药效的健康食品.苹果酸(2羟基丁二酸)是这种饮料的主要成分,苹果酸的结构简式如图所示.下列说法不正确的是( )
苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等药效的健康食品.苹果酸(2羟基丁二酸)是这种饮料的主要成分,苹果酸的结构简式如图所示.下列说法不正确的是( )
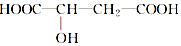 苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等药效的健康食品.苹果酸(2羟基丁二酸)是这种饮料的主要成分,苹果酸的结构简式如图所示.下列说法不正确的是( )
苹果醋是一种由苹果发酵而形成的具有解毒、降脂、减肥等药效的健康食品.苹果酸(2羟基丁二酸)是这种饮料的主要成分,苹果酸的结构简式如图所示.下列说法不正确的是( )| A. | 苹果酸在一定条件下能发生酯化反应 | |
| B. | 苹果酸在一定条件下能发生催化氧化反应 | |
| C. | 1 mol苹果酸与足量Na反应生成33.6 L H2(标准状况下) | |
| D. | 1 mol苹果酸与过量的Na2CO3溶液反应可生成1molCO2 |
4.氰气[(CN)2]和氰化物都是剧毒性物质,氰分子的结构式为N≡C-C≡N,性质与卤素相似,下列叙述错误的是( )
| A. | 氰分子中四原子共直线,是非极性分子 | |
| B. | 氰分子中C≡N键长大于C≡C键长 | |
| C. | 氰气分子中含有σ键和π键 | |
| D. | 氰化氢在一定条件下能与烯烃发生加成反应 |
14.下列化合物的用途叙述正确的是( )
| A. | 光纤通信使用的光缆主要成分是晶体Si | |
| B. | 水玻璃可用作防火剂或防腐剂 | |
| C. | 氯水、酒精能杀菌消毒,都利用了强氧化性 | |
| D. | SO2可用来漂白纸浆、毛、草帽、增白食品等 |
18.化学与生产、生活、社会可持续发展密切相关.下列说法正确的是( )
| A. | 推广使用一次性木筷,减少疾病传染 | |
| B. | 将地沟油回收重新加工为食用油,提高资源的利用率 | |
| C. | 推广使用电动汽车、天然气汽车等公共交通工具,保护环境 | |
| D. | 推广使用煤的气化、液化技术可减少二氧化碳等温室气体的排放 |
13.常温常压时烯烃与氢气混合不反应,高温时反应很慢,但在适当的催化剂存在时可与氢气反应生成烷,
一般认为加氢反应是在催化剂表面进行.反应过程的示意图如下:

下列说法中正确的是( )
一般认为加氢反应是在催化剂表面进行.反应过程的示意图如下:

下列说法中正确的是( )
| A. | 乙烯和H2生成乙烷的反应△H>0 | |
| B. | 加入催化剂,降低了E活,并减小了反应的△H | |
| C. | 图1表明,催化加氢过程中催化剂参与反应过程并形成不稳定的中间体 | |
| D. | 图2表明,催化加氢过程中催化剂将较难发生的反应分成了多个容易发生的反应,可提高反应物的转化率 |