题目内容
某元素X的相对原子质量为a,它的最高价氧化物的水化物的化学式为HmXOn(m>1).下列有关叙述中一定正确的是( )
| A、该酸的水溶液中c(H+):c(XOnm-)=n:1 |
| B、该酸的摩尔质量为(m+a+16n)g |
| C、100mL该酸溶液,只能中和4gNaOH |
| D、若0.1molL-1该酸溶液的pH=1,则NamXOn的水溶液的pH>7 |
考点:弱电解质在水溶液中的电离平衡,摩尔质量
专题:
分析:A、根据HmXOn可能是多元弱酸解答;
B、摩尔质量的单位为g/mol;
C、根据n=cV计算HmXOn的物质的量,再结合反应本质OH-+H+=H2O计算;
D、若0.1 mol?L-1的HmXOn溶液的pH=1,溶液中c(H+)=0.1mol/L<mmol/L,故HmXOn为弱酸.
B、摩尔质量的单位为g/mol;
C、根据n=cV计算HmXOn的物质的量,再结合反应本质OH-+H+=H2O计算;
D、若0.1 mol?L-1的HmXOn溶液的pH=1,溶液中c(H+)=0.1mol/L<mmol/L,故HmXOn为弱酸.
解答:
解:A、若HmXOn是多元弱酸,电离出的(XOnm-)很小,溶液中n(H+):n(XOnm-)远远大于m:1,故B错误;
B、摩尔质量的单位为g/mol,故B错误;
C、1L 0.1mol?L-1的HmXOn溶液中HmXOn的物质的量为1L×0.1mol/L=0.1mol,结合OH-+H+=H2O可知,中和氢氧化钠的物质的量为0.1mol×m=mmol,故C错误;
D、若0.1 mol?L-1的HmXOn溶液的pH=1,溶液中c(H+)=0.1mol/L<mmol/L,故HmXOn为弱酸,0.1 mol?L-1NamXOn溶液中XOnm-离子水解,溶液呈碱性,故溶液的pH>7,故D正确;
故选D.
B、摩尔质量的单位为g/mol,故B错误;
C、1L 0.1mol?L-1的HmXOn溶液中HmXOn的物质的量为1L×0.1mol/L=0.1mol,结合OH-+H+=H2O可知,中和氢氧化钠的物质的量为0.1mol×m=mmol,故C错误;
D、若0.1 mol?L-1的HmXOn溶液的pH=1,溶液中c(H+)=0.1mol/L<mmol/L,故HmXOn为弱酸,0.1 mol?L-1NamXOn溶液中XOnm-离子水解,溶液呈碱性,故溶液的pH>7,故D正确;
故选D.
点评:本题考查常用化学计量的有关计算、弱电解质的电离、盐类水解等,难度中等,注意B中根据酸的强弱进行解答.

练习册系列答案
相关题目
在一定的温度下,可逆反应A(g)+3B(g)?2C(g)达到平衡的标志是( )
| A、A、B、C的分子数相等 |
| B、A、B、C的浓度相等 |
| C、单位时间生成n mol A,同时生成2n mol C |
| D、A、B、C的分子数之比为1:3:2 |
下列各组中的离子,能在无色酸性溶液中大量共存的是( )
| A、Na+、Mg2+、Cl-、HCO3- |
| B、K+、Cu2+、SO42-、NO3- |
| C、K+、Na+、OH-、Cl- |
| D、Mg2+、Al3+、NO3-、SO42- |
25℃时,向VmLpH=a的硫酸中滴加10V mL pH=b的NaOH溶液时,溶液中SO42-的物质的量恰好等于加入的Na+的物质的量的
,则a+b的值为( )
| 1 |
| 2 |
| A、13 | B、14 |
| C、15 | D、不能确定 |
据下列反应判断有关物质的氧化性顺序正确的是( )
①F2+2NaCl(熔融)═2NaF+Cl2 ②Cl2+2NaBr═2NaCl+Br2 ③Br2+2NaI═2NaBr+I2.
①F2+2NaCl(熔融)═2NaF+Cl2 ②Cl2+2NaBr═2NaCl+Br2 ③Br2+2NaI═2NaBr+I2.
| A、F2>Br2>I2>Cl2 |
| B、I2>Br2>Cl2>F2 |
| C、F2>Cl2>Br2>I2 |
| D、NaI>NaBr>NaCl>NaF |
需要加入还原剂才能使下列离子反应发生的是( )
| A、MnO4-~Mn2+ |
| B、Br-~Br2 |
| C、CO32-~CO2 |
| D、S2-~S |
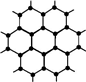 石墨烯是从石墨中剥离出的单层石墨.这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为是目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,应用前景十分广阔.下列关于石墨烯的叙述中正确的是( )
石墨烯是从石墨中剥离出的单层石墨.这种“只有一层碳原子厚的碳薄片”的石墨烯,被公认为是目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,应用前景十分广阔.下列关于石墨烯的叙述中正确的是( )| A、石墨烯是碳单质 |
| B、石墨烯是一种有机物 |
| C、石墨烯中碳原子的化合价为+3 |
| D、石墨烯可导电,说明碳原子之间形成离子键 |