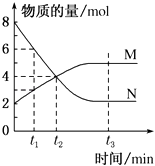
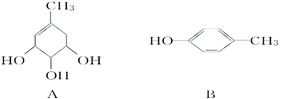
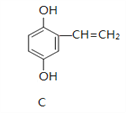
��Ŀ����
����Ŀ��Ϊ��֤��Ԫ�صķǽ����Ա���Ԫ�صķǽ�����ǿ��ij��ѧʵ��С�����������ʵ�飬��ش��������⣺ 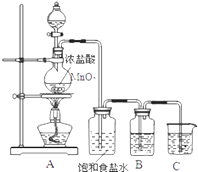
��1��װ��B��ʢ�ŵ��Լ�������ѡ���ʵ������Ϊ �� ��ѧ��Ӧ����ʽ�� ��
A��Na2S��Һ B��Na2SO3��Һ C��Na2SO4��Һ
��2��װ��C��ʢ���ռ�ϡ��Һ��Ŀ���� ��
��3����֤����Ԫ�ر���Ԫ�طǽ�����ǿ������Ϊ �� ������ţ�
����ԭ�ӱ���ԭ�Ӹ�����õ����γ����ӣ�
�ڴ�����������Ա�ϡ����ǿ��
��S2����Cl����ԭ��ǿ��
��HCl��H2S�ȶ���
��4����Bƿ��ʢ��KI��Һ��CCl4�Լ���ʵ��������ã�����ֵ�ʵ������ �� д����Ӧ�����ӷ���ʽ ��
���𰸡�
��1��A����������ɫ������Na2S+Cl2=2NaCl+S��
��2��������������ֹ��Ⱦ����
��3���٢ۢ�
��4���²�Ϊ��ɫ��2I��+Cl2=2Cl��+I2
���������⣺��1��Ҫ��C�з��������û�����ķ�Ӧ���ڸ����Լ���ֻ��ѡȡNa2S��Һ�����������û���Ӧ�����ӷ���ʽΪ��Cl2+S2���T2Cl��+S������Ӧ���е���ɫ�������������Դ��ǣ�A����������ɫ������Na2S+Cl2=2NaCl+S������2������Ϊ�ж����壬Ҫ����β��������������������������Һ��Ӧ������װ��C��ʢ���ռ���Һ��������������������ֹ��Ⱦ���������Դ��ǣ�������������ֹ��Ⱦ��������3����֤����Ԫ�ر���Ԫ�طǽ�����ǿ�����ݢ���ԭ�ӱ���ԭ�Ӹ�����õ����γ����ӣ��õ�������Խǿ�ǽ�����Խǿ������ȷ����ͨ����ۺ���������Կ��ԱȽϷǽ����ԣ����ܱȽ��������ԣ��ʴ����S2����Cl����ԭ��ǿ�����������ӵĻ�ԭ��Խ���ǽ�����Խǿ���жϣ�����ȷ���⻯��Խ�ȶ����ǽ�����Խǿ������ȷ�����Ԣ٢ۢܣ����Դ��ǣ��٢ۢܣ���4��������⻯�ط�Ӧ���ɵ��ʵ⣬��CCl4�Լ�����Һ��ֲ㣬�²�Ϊ�ⵥ�ʺ�CCl4 �� �����²����ɫ���䷴Ӧ�����ӷ���ʽΪ��2I��+Cl2=2Cl��+I2 �� ���Դ��ǣ��²�Ϊ��ɫ��2I��+Cl2=2Cl��+I2 ��
�����㾫����������Ĺؼ���������ǽ�����Ԫ�����ڱ��е�λ�ü������ʵݱ�Ĺ��ɵ����֪ʶ��������Ŀǰ��֪��112��Ԫ���У��ǽ���Ԫ����22�֣���H��ǽ���Ԫ�ض�λ�����ڱ������Ϸ���H�����Ϸ�����F�Ƿǽ�������ǿ��Ԫ�أ�

 ��Ч���ܿ�ʱ��ҵϵ�д�
��Ч���ܿ�ʱ��ҵϵ�д� �ݾ�ѵ������ϵ�д�
�ݾ�ѵ������ϵ�д� С����ȫ�ܼ��ϵ�д�
С����ȫ�ܼ��ϵ�д�����Ŀ���ⶨCuSO4��xH2O�����xֵ�������������ʾ����֪x������ֵΪ5.0���������Ŀ���ԭ����
�������� | ����+���� | ʧˮ������+���� |
11.70g | 20.82g | 16.50g |
A. �����к����ӷ����� B. δ�����ز���
C. ����ʱ�о��彦�� D. ����ǰ����δ��ĥ