题目内容
12.若NA 表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 标准状况下,11.2LH2O含有的分子数为0.5NA | |
| B. | 7.8g过氧化钠与足量水反应,转移电子数为0.2NA | |
| C. | 常温常压下,6gO2和26gO3混合气体中的原子总数为2NA | |
| D. | 100mL0.1mol/L的Na2SO4溶液中,所含离子总数为0.2NA |
分析 A.气体摩尔体积使用对象为气体;
B.根据过氧化钠的物质的量和O元素的化合价分析;
C.氧气和臭氧都是由氧原子构成,依据氧元素质量计算氧原子物质的量及个数;
D.求出Na2SO4的物质的量n=CV,然后根据1molNa2SO4中含2mol钠离子和1mol硫酸根离子来分析;
解答 解:A.标况下水是液体,不能使用气体摩尔体积,故A错误;
B.7.8g过氧化钠为0.1mol,与足量水反应,自身发生氧化还原反应,转移电子数为0.1NA,故B错误;
C.6gO2和26gO3混合气体,含有氧元素质量为:32g,含有氧原子个数为:$\frac{32g}{16g/mol}$×NA=2NA,故C正确;
D.100mL0.1mol/L的Na2SO4溶液中,含有硫酸钠的物质的量为0.1L×0.1mol/L=0.01mol,含有钠离子0.02mol,硫酸根离子0.01mol,所含离子总数为0.03NA,故D错误;
故选:C.
点评 本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,注意气体摩尔体积使用条件和对象,题目难度不大.

练习册系列答案
相关题目
2.下列有关实验装置的说法正确的是( )
| A. | 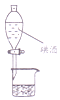 用图装置分离该酒中的碘和酒精 | B. | 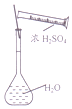 用图装置配制稀硫酸 | ||
| C. |  用图装置由食盐水制得食盐晶体 | D. | 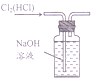 用图装置除去Cl2中的HCl |
3.下列有关分枝酸的叙述中,正确的是( )


| A. | 分子中含有2种官能团 | |
| B. | 一定条件下,能与乙醇或乙酸发生相同类型的反应 | |
| C. | 1mol分枝酸最多可与3molNaOH发生反应 | |
| D. | 可运用同一原理分别使溴的四氯化碳溶液与酸性高锰酸钾溶液褪色 |
20.下列有关实验装置进行的相应实验,能达到实验目的是( )
| A. |  用图所示装设测定一定时间内生成SO2的反应速率 | |
| B. | 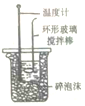 用图所示装置测定稀H2SO4和稀Ca(OH)2的中和热 | |
| C. | 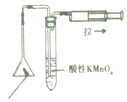 用图所示装置检验火柴燃烧产生的SO2 | |
| D. | 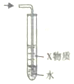 如图装置中X若为苯,可用于吸收NH3或HC1,并防止倒吸 |
7.设NA表示阿伏加德罗常数的数值,则下列说法中正确的是( )
| A. | 常温常压下,8.0gCH4中含有的氢原子数为NA | |
| B. | 1mol氯气跟水完全反应,转移的电子数为2NA | |
| C. | 1 molNa2O2跟足量CO2完全反应,转移的电子数为NA | |
| D. | 0.1mol/L MgCl2溶液中含氯离子数为0.2NA |
17.水解反应与社会、生活密切相关.对下列现象、事实或解释不正确的是( )
| 选项 | 现象或事实 | 解释 |
| A | 泡沫灭火器(含有NaHCO3与硫酸铝)灭火 | 3HCO3-+Al3+=Al(OH)3↓+3CO2↑ |
| B | 将AlCl3溶液加热、蒸干、灼烧,可的导固体Al2O3 | 加热促进了AlCl水解 |
| C | 施肥时,草木灰(有效成分为K2CO3)与NH4Cl混合使用 | 同时使用氮肥和钾肥效果更好 |
| D | 配制SnCl2溶液时,先用盐酸酸化蒸馏水,然后加入SnCl2晶体 | 盐酸抑制SnCl2水解 |
| A. | A | B. | B | C. | C | D. | D |
4.若在加入铝粉能产生氢气的无色溶液中,分别加入下列各组离子,可能共存的是( )
| A. | NH4+、NO3-、Al3+、Cl- | B. | Na+、AlO2-、K+、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | AlO2-、K+、NO3-、OH- |
15.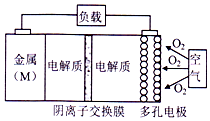 电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
 电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )
电池的“理论比能量”指单位质量的电极材料理论上能释放的最大电能.“金属(M)〜空气电池”(如下图)具有原料易得、能量密度高等优点.该类电池放电的总反应方程式为:4M+nO2+2nH2O═4M(OH) n.下列说法不正确的是( )| A. | “金属(M)〜空气电池”放电过程的正极反应式:O2+2H2O+4e-=4M(OH)n | |
| B. | 比较Mg、Al、Zn三种“金属-空气电池”,“Al-空气电池”的理论比能量最高 | |
| C. | 电解质溶液中的阴离子从负极区移向正极区 | |
| D. | 在“M-空气电池”中,为防止负极区沉积Mg(OH)2,宜采用中性电解质及阳离子交换膜 |
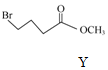
16.合成药物异搏定路线中某一步骤如图:
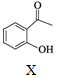 +
+ $\stackrel{HaH,DMF}{→}$
$\stackrel{HaH,DMF}{→}$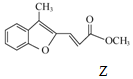 ,下列说法不正确的是( )
,下列说法不正确的是( )
 +
+ $\stackrel{HaH,DMF}{→}$
$\stackrel{HaH,DMF}{→}$ ,下列说法不正确的是( )
,下列说法不正确的是( )| A. | 物质X中所有碳原子可能共平面 | |
| B. | 可用FeCl3溶液鉴别Z中是否含有X | |
| C. | 等物质的量的X、Z分别与H2加成,最多消耗H2的物质的量之比为3:5 | |
| D. | 等物质的量的Y、Z分别与NaOH溶液反应,最多消耗NaOH的物质的量之比为1:1 |