题目内容
向一个小烧杯中加入20克蔗糖,加3~4滴水,再加入20ml浓硫酸,观察到的实验现象是:烧杯发热、蔗糖变黑、体积膨胀,变成疏松多孔的海棉状的炭,并放出有制激性气味的气体。这个过程中浓硫酸没有表现出的性质是
- A.吸水性
- B.脱水性
- C.强氧化性
- D.酸性
D
答案:D
烧杯发热,说明浓硫酸有吸水性、蔗糖变黑,说明浓硫酸有脱水性、变成疏松多孔的海棉状的炭,并放出有制激性气味的气体,说明浓硫酸有强氧化性。
答案:D
烧杯发热,说明浓硫酸有吸水性、蔗糖变黑,说明浓硫酸有脱水性、变成疏松多孔的海棉状的炭,并放出有制激性气味的气体,说明浓硫酸有强氧化性。

练习册系列答案
相关题目
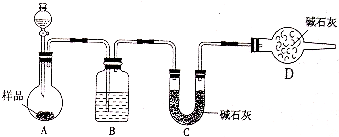
 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.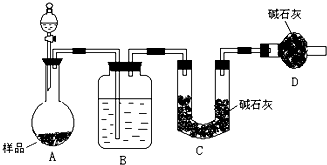 某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.
某校化学研究学习小组设计如下实验方案,测定小苏打样品中纯碱的质量分数.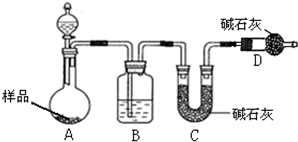 为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案:
为测定碳酸钠与碳酸氢钠混合物样品中碳酸钠的质量分数,设计如下实验方案: