题目内容
8.向盛有10g Na2O2固体的容器中充入一定体积的CO2气体,发生反应后测得固体质量为12.8g,求反应后容器内固体的成分和质量.分析 发生2CO2+2Na2O2=2Na2CO3+O2,固体增重质量为12.8g-10g=2.8g,结合差量法计算.
解答 解:发生2CO2+2Na2O2=2Na2CO3+O2,设生成碳酸钠的质量为xg,则
2CO2+2Na2O2=2Na2CO3+O2,△m
212 56
x (12.8g-10g)
$\frac{212}{x}=\frac{56}{(12.8g-10g)}$,解得x=10.6g,
则反应后还存在过氧化钠的质量为12.8g-10.6g=2.2g,
答:反应后容器内固体的成分为碳酸钠、过氧化钠,质量分别为10.6g、2.2g.
点评 本题考查化学反应的计算,为高频考点,把握发生的反应及差量法计算为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
18.下列物质中,含氢原子数目最多的是( )
| A. | 0.9 mol H2O | B. | 0.3 mol H2SO4 | C. | 0.2 mol NH3 | D. | 0.4 mol CH4 |
16.某有机物的结构简图如图,它有几种官能团( )


| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
20.下列有关铝的化合物的说法正确的是( )
| A. | 氧化铝坩埚可用于熔融NaOH实验 | |
| B. | 氧化铝的熔点很高,是一种较好的耐火材料 | |
| C. | 明矾可用于自来水的消毒 | |
| D. | 氢氧化铝能中和胃酸,适合于胃溃疡患者服用 |
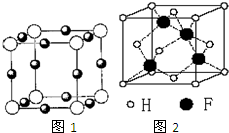 已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)
已知A、B、C、D、E、F都是周期表中前四周期的元素,它们的核电荷数A<B<C<D<E<F.其中A原子核外有三个未成对电子;化合物B2E的晶体为离子晶体,E原子核外的M层中只有两对成对电子;C元素是地壳中含量最高的金属元素;D单质的晶体类型在同周期的单质中没有相同的;F原子核外最外层电子数与B相同,其余各层电子均充满.请根据以上信息,回答下列问题:(答题时,A、B、C、D、E、F用所对应的元素符号表示)