题目内容
19.下列化学反应中,属于氧化还原反应的是( )| A. | SO3+H2O═H2SO4 | B. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑ | ||
| C. | Zn+H2SO4═ZnSO4+H2↑ | D. | AgNO3+HCl═AgCl↓+HNO3 |
分析 含元素化合价变化的反应,为氧化还原反应,以此来解答.
解答 解:A、B、D中均没有元素的化合价变化,均为非氧化还原反应,只有C中Zn、H元素的化合价变化,为氧化还原反应,
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,注意元素化合价的判断,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.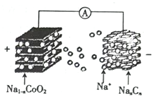 室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:
室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:
NaCoO2+Cn$?_{放电}^{充电}$Na2-xCoO2+NaxCn
其电池结构如图所示.下列说法不正确的是( )
 室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:
室温钠离子电池具有资源丰富,成本低,能量转换效率高、寿命等优势.一种用碳基材料(NaxCn)作负极的可充电钠离子电池的瓜原理如下:NaCoO2+Cn$?_{放电}^{充电}$Na2-xCoO2+NaxCn
其电池结构如图所示.下列说法不正确的是( )
| A. | 充电时,Na+向正极移动 | |
| B. | 放电时,负极的电极反应式为NaxCn-xe-=xNa++Cn | |
| C. | 充电时,阴极质量减小 | |
| D. | 充电时,阳极的电极反应式为NaCoO2-xe-=Na1-xCoO2+xNa+ |
7.下列说法正确的是( )
| A. | PCl5 分子中所有原子都满足最外层8电子稳定结构且共用电子对发生偏移 | |
| B. | 两个原子间形成共价键时,最多可以有两个σ键 | |
| C. | H3O+中H-O-H的键角比H2O中H-O-H的键角大 | |
| D. | 酸性强弱比较:HClO>HClO2 |
4.${\;}_{8}^{16}$O、${\;}_{8}^{18}$O、O2-、O2、O3是( )
| A. | 氧的五种同位素 | B. | 五种氧元素 | ||
| C. | 氧的五种同素异形体 | D. | 氧元素的五种不同微粒 |
8.在电解池中,阴极上发生的反应是( )
| A. | 还原反应 | B. | 氧化反应 | C. | 失去电子被氧化 | D. | 得到电子被氧化 |
9.现有部分短周期元素的性质或原子结构如下表:
(1)元素X位于元素周期表的第二周期第IVA族,它的一种核素可测定文物年代,这种核素的符号是146C.
(2)元素Y的原子结构示意图为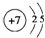 ,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子.
,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子.
(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应.
| 元素编号 | 元素性质或原子结构 |
| T | M层上电子数是K层上电子数的3倍 |
| X | 最外层电子数是次外层电子数的2倍 |
| Y | 常温下单质为双原子分子,其氢化物水溶液呈碱性 |
| Z | 元素最高正价是+7价 |
(2)元素Y的原子结构示意图为
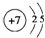 ,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子.
,与氢元素形成一种离子YH4+,写出某溶液中含有该微粒的检验方法取少量样品放入试管,加入氢氧化钠溶液,加热,产生能使湿润的红色石蕊试纸变蓝的气体,证明有铵根离子.(3)元素Z与元素T相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是b
a.常温下Z的单质和T的单质状态不同
b.Z的氢化物比T的氢化物稳定
c.一定条件下Z和T的单质都能与氢氧化钠溶液反应.