题目内容
20.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 标准状况下,11.2 L CCl4中含有的C Cl键的个数为2NA | |
| B. | 1 mol Na2O和Na2O2中含有的阴、阳离子总数是3 NA | |
| C. | 常温下,0.1 mol Cl2通入NaOH溶液中充分反应,转移电子数为0.2 NA | |
| D. | 1 L 0.1 mol•L-1氨水溶液中所含的离子和分子总数大于0.1 NA但小于0.2 NA |
分析 A、标况下四氯化碳为液体;
B、氧化钠和过氧化钠均由2个阳离子和1个阴离子构成;
C、氯气和碱的反应为歧化反应;
D、氨水溶液中的微粒有NH3•H2O、NH4+、OH-、H+、H2O等.
解答 解:A、标准状况下四氯化碳不是气态,不能适用于气体摩尔体积,即标准状况下,11.2 L CCl4中含有的C-Cl键的个数一定不是2NA,故A错误;
B、氧化钠和过氧化钠中阴阳离子的个数之比均是1:2,则1 mol Na2O和Na2O2中含有的阴、阳离子总数是3 NA,故B正确;
C、氯气与氢氧化钠的反应中氯气既是氧化剂,也是还原剂,转移1个电子.常温下,0.1 mol Cl2通入NaOH溶液中充分反应,转移电子数为0.1NA,故C错误;
D、1 L 0.1 mol•L-1氨水溶液中所含的离子和分子总数大于0.1 NA,因为还含有大量的水分子,故D错误.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.

练习册系列答案
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
10.下列叙述正确的是( )
| A. | 碳族元素都是非金属元素,其非金属性随核电荷数的增加而减弱 | |
| B. | 石英、水晶、硅石的主要成分都是二氧化硅 | |
| C. | 二氧化硅的化学性质活泼,能与任意的酸、碱发生反应 | |
| D. | 碳族元素的单质都有导电性 |
11.燃烧由CH4和C3H8组成的混合气体,生成3.52gCO2和1.98gH2O.此混合气体中CH4与C3H8的体积比为( )
| A. | 1:5 | B. | 1:2 | C. | 3:2 | D. | 2:1 |
8.常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 0.1 mol•L-1 KSCN溶液中:Fe3+、NH4+、Br-、SO42- | |
| B. | $\frac{{c(O{H^-})}}{{c({H^+})}}$=106的溶液中:NH4+、K+、AlO2-、NO3- | |
| C. | 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42-、Cl- | |
| D. | 0.1 mol•L-1 Ca(NO3)2溶液中:Na+、NH4+、CO32-、CH3COO- |
12.对于有机物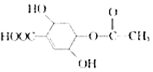 的叙述中不正确的是( )
的叙述中不正确的是( )
 的叙述中不正确的是( )
的叙述中不正确的是( )| A. | 该物质能发生水解反应,1 mol该有机物能与2mo1的NaOH反应 | |
| B. | 该物质可使溴水褪色 | |
| C. | 该物质与Na2CO3溶液反应放出CO2 | |
| D. | 该物质遇FeCl3溶液显色 |
9.下列指定溶液中,一定能够大量共存的离子组是( )
| A. | 由水电离产生的两种离子浓度关系为c(H+)•c(OH-)=10-24的溶液中:Al3+、Na+、Cl-、SO42- | |
| B. | 含有大量AlO2-的溶液中:HCO3-、K+、Cl-、NO3- | |
| C. | 常温下,PH=7的溶液中:Fe3+、Na+、NO3-、SO42- | |
| D. | 能使广泛PH试纸显蓝色的溶液中:K+、Ba2+、Cl-、Br- |
1.若将基态P原子的电子排布式写成1s22s22p63s23px23py1,它违背了( )
| A. | 泡利原理 | B. | 能量守恒原理 | C. | 构造原理 | D. | 洪特规则 |