题目内容
已知:2H2(g) +O2(g) = 2H2O(g) ΔH =-483.6 kJ/mol
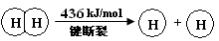

下列说法不正确的是
A.H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固
B.H2O(g)=H2(g) + 1/2O2(g) ΔH = +241.8 kJ/mol
C.破坏1 mol H—O 键需要的能量是463.4 kJ
D.H2(g) + 1/2O2(g)=H2O(l) ΔH <-241.8 kJ/mol
A
【解析】
试题分析:A.2个氢分子中的H—H和1个氧分子中的O=O键断裂化学键吸收能量,形成2个水分子中的4个H—O键释放能量。由于该反应放出能量,说明反应物的总能量高于生成物,但是不能说H2(g) 中的H—H 键比 H2O(g) 中的H—O 键牢固,错误;B.热化学方程式表示2mol的H2和1mol的O2发生反应产生2mol的气态水,会放出热量483.6 kJ ,则产生1mol的气态水放出热量是241.8KJ的能量,由于形成水和水分解是相反的过程,所以1mol的气态水分解产生1mol的H2(g) 和1/2molO2(g) 吸收热量是483.6 kJ,正确;C.破坏1 mol H—O 键需要的能量是463.4 kJ,正确;D.由于液态水含有的能量比气态水少,所以1mol的H2(g) 和 1/2mol的O2(g)反应产生1mol的液态H2O(l) 放出的热量大于241.8 kJ,所以 ΔH <-241.8 kJ/mo,正确。
考点:考查反应热与键能、物质的状态及物质的多少的关系的知识。

 智能训练练测考系列答案
智能训练练测考系列答案根据表中信息判断,下列选项不正确的是
序号 | 反应物 | 产物 |
① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
② | Cl2、FeBr2 | FeCl3、FeBr3 |
③ | MnO4- | Cl2、Mn2+ |
A.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol

 等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫。
等)制备碱式硫酸铝[Al2(SO4)x(OH)6-2x]溶液,并用于烟气脱硫。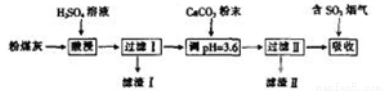
 B.质子数为6、质量数为14的原子:
B.质子数为6、质量数为14的原子:
 D.氯的原子结构示意图:
D.氯的原子结构示意图:
