题目内容
1.设NA表示阿伏加德罗常数,下列说法正确的是( )| A. | 23g钠与足量氧气充分反应,转移的电子个数为NA | |
| B. | 将1molFeCl3水解制成胶体,所得胶体的微粒数为NA | |
| C. | 1mol Na2O2与水完全反应时转移电子数为2NA | |
| D. | NA个一氧化碳分子和0.5 mol甲烷的质量比为7:4 |
分析 A.钠为+1价金属,23g钠为1mol,完全反应失去1mol电子;
B.氢氧化铁胶体为氢氧化铁的聚集体,无法计算胶粒数目;
C.1mol过氧化钠完全反应生成0.5mol氧气,过氧化钠中氧元素的化合价为-1价,据此判断转移电子数;
D.NA个一氧化碳分子的物质的量为1mol,质量为28g;0.5 mol甲烷的质量为8g.
解答 解:A.23g钠的物质的量为:$\frac{23g}{23g/mol}$=1mol,1mol钠完全反应失去1mol电子,转移的电子个数为NA,故A正确;
B.将1molFeCl3水解制成胶体,由于氢氧化铁胶粒为氢氧化铁聚集体,则含有胶粒的物质的量小于1mol,所得胶体的微粒数小于NA,故B错误;
C.1mol过氧化钠与水完全反应生成0.5mol氧气,转移了1mol电子,转移电子数为NA,故C错误;
D.NA个一氧化碳分子的物质的量为1mol,质量为:28g/mol×1mol=28g,0.5 mol甲烷的质量为8g,二者的质量比为:28g:8g=7:2,故D错误;
故选A.
点评 本题考查阿伏加德罗常数的应用,题目难度中等,注意熟练掌握以物质的量为中心的各化学量与阿伏加德罗常数的关系,明确过氧化钠中氧元素的化合价为-1价;B为易错点,注意氢氧化铁胶粒为氢氧化铁的聚集体.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案
相关题目
12.下列说法正确的是( )
| A. | 凡金属跟非金属元素化合时都能形成离子键 | |
| B. | 离子化合物熔融状态下一定导电 | |
| C. | 离子化合物中的阳离子只能是金属离子,酸根离子中不能含有金属元素 | |
| D. | 溶于水可以导电的化合物一定是离子化合物 |
9.下面几组物质,请将合适组号填写在下表中.
①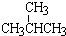 和
和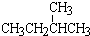 ; ②
; ②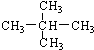 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
①
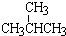 和
和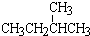 ; ②
; ②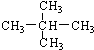 和
和 ; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).
; ③CH4和CH3CH2CH3;④金刚石与石墨;⑤氕、氘与氚;⑥16O、17O和18O;⑦乙醇(CH3CH2OH)和二甲醚(CH3OCH3);⑧氧气(O2)与臭氧(O3).| 类别 | 同位素 | 同系物 | 同素异形体 | 同分异构体 |
| 组号 | ⑤⑥ | ①③ | ④⑧ | ②⑦ |
6.我国有丰富的天然气资源.以天然气为原料合成尿素的主要步骤如图所示(图中某些转化步骤及生成物未列出):

(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是BD.
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的
变化如下:
提高氢碳比[$\frac{n({H}_{2}O)}{n(CO)}$],K值不变(填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正)>v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是A.
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为2:1,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为有利于提高CO2的转化率,因为NH3极易溶于水,便于分离、回收利用.
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成4.8×108L 氨气.(假设体积均在标准状况下测定)

(1)“造合成气”发生的热化学方程式是CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0在恒温恒容的条件下,欲提高CH4的反应速率和转化率,下列措施可行的是BD.
A、增大压强 B、升高温度 C、充入He气 D、增大水蒸气浓度
(2)“转化一氧化碳”发生的方程式是H2O(g)+CO(g)?H2(g)+CO2(g),该反应平衡常数随温度的
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
提高氢碳比[$\frac{n({H}_{2}O)}{n(CO)}$],K值不变(填“增大”、“不变”或“减小”);若该反应在400℃时进行,起始通入等物质的量的H2O和CO,反应进行到某一时刻时CO和CO2的浓度比为1:3,此时v(正)>v(逆)(填“>”、“=”或“<”).
(3)有关合成氨工业的说法中正确的是A.
A、该反应属于人工固氮
B、合成氨工业中使用催化剂能提高反应物的利用率
C、合成氨反应温度控制在500℃左右,目的是使化学平衡向正反应方向移动
D、合成氨工业采用循环操作的主要原因是为了加快反应速率
(4)生产尿素过程中,理论上n(NH3):n(CO2)的最佳配比为2:1,而实际生产过程中,往往使n(NH3):n(CO2)≥3,这是因为有利于提高CO2的转化率,因为NH3极易溶于水,便于分离、回收利用.
(5)当甲烷合成氨气的转化率为60%时,以3.0×108L甲烷为原料能够合成4.8×108L 氨气.(假设体积均在标准状况下测定)
13.人的血液里Ca2+的浓度一般采用g•cm-3表示,今抽一血样20.00mL加入适量的草酸铵[(NH4)2C2O4]溶液,可析出CaC2O4沉淀,将沉淀洗净后溶于强酸可得草酸,再用浓度为0.02mol•L-1的KMnO4溶液滴定.当观察到溶液紫色褪尽时,共消耗12.00mL KMnO4溶液.则该血液样品中Ca2+的浓度为( )
| A. | 0.0015 g•cm-3 | B. | 0.0012 g•cm-3 | C. | 0.0024 g•cm-3 | D. | 0.002 g•cm-3 |
10.下列有关说法错误的是( )
| A. | 已知氯化钴及其水合物会呈现不同颜色(如下),德国科学家发明了添加氯化钴的变色水泥,据此推测雨天变色水泥呈粉红色 | |
| B. | 已知铬酸根(黄色)和重铬酸根(橙色)离子间存在如下平衡:2CrO42-+2H+?Cr2O72-+H2O,若加水稀释,则溶液中所有离子浓度均减少 | |
| C. | 若反应2A(g)+B(s)?C(g)+3D(g)只有高温下才能自发进行,则该反应的△H>0 | |
| D. | 增大反应物的浓度,可使单位体积内活化分子数目增多,反应速率加快 |
11.下列离子方程式正确的是( )
| A. | 石灰乳与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| B. | AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| C. | NaHCO3和过量的澄清石灰水反应:2HCO3-+2OH-+Ca2+═CaCO3↓+CO32-+2H2O | |
| D. | NH4HSO3溶液与足量NaOH溶液混合加热:NH4++HSO3-+2OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+SO32-+2H2O |
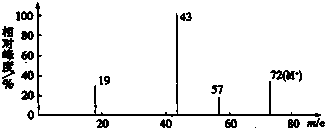
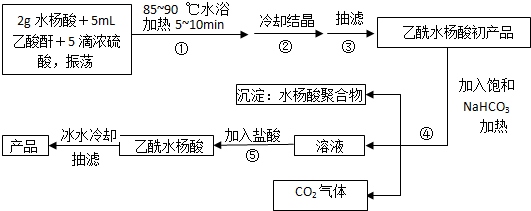
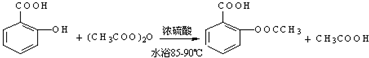 ;反应类型取代反应;
;反应类型取代反应; 、
、 ;
; ;
;