题目内容
用NA代表阿伏加德罗常数值.下列说法正确的是
- A.2.3g钠在空气中加热反应时,失去的电子数为0.2NA
- B.标准状况下,1.12L的HCHO所含的原子数为0.2NA
- C.28g C2H4和C4H8混合物中所含的分子数为3NA
- D.1mol FeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒
B
分析:A、质量换算物质的量,计算失去电子数,钠加热反应生成过氧化钠;
B、根据气体摩尔体积的条件应用计算判断;
C、依据质量和摩尔质量换算物质的量计算分子数;
D、胶体微粒是氢氧化铁的集合体;
解答:A、2.3g钠物质的量为0.1mol,完全反应转移电子数为0.1NA,故A错误;
B、标准状况下,甲醛是气体,1.12L的HCHO物质的量为0.05mol,含原子数为0.05mol×4×NA=0.2NA,故B正确;
C、28g C2H4和C4H8混合物中含分子数,若全是C2H4分子数=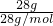 ×NA=NA,若全是C4H8分子数=
×NA=NA,若全是C4H8分子数= =0.5mol,所以28g C2H4和C4H8混合物中含分子数在0.5NA-NA间,故C错误;
=0.5mol,所以28g C2H4和C4H8混合物中含分子数在0.5NA-NA间,故C错误;
D、Fe(OH)3胶粒是氢氧化铁的微粒集合体,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,质量换算物质的量计算微粒数,气体摩尔体积的条件应用,胶体微粒的组成,熟练掌握概念和计算,即可解决.
分析:A、质量换算物质的量,计算失去电子数,钠加热反应生成过氧化钠;
B、根据气体摩尔体积的条件应用计算判断;
C、依据质量和摩尔质量换算物质的量计算分子数;
D、胶体微粒是氢氧化铁的集合体;
解答:A、2.3g钠物质的量为0.1mol,完全反应转移电子数为0.1NA,故A错误;
B、标准状况下,甲醛是气体,1.12L的HCHO物质的量为0.05mol,含原子数为0.05mol×4×NA=0.2NA,故B正确;
C、28g C2H4和C4H8混合物中含分子数,若全是C2H4分子数=
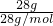 ×NA=NA,若全是C4H8分子数=
×NA=NA,若全是C4H8分子数= =0.5mol,所以28g C2H4和C4H8混合物中含分子数在0.5NA-NA间,故C错误;
=0.5mol,所以28g C2H4和C4H8混合物中含分子数在0.5NA-NA间,故C错误;D、Fe(OH)3胶粒是氢氧化铁的微粒集合体,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,质量换算物质的量计算微粒数,气体摩尔体积的条件应用,胶体微粒的组成,熟练掌握概念和计算,即可解决.

练习册系列答案
相关题目