题目内容
13C-NMR(核磁共振)、15N-NNR可用于测定蛋白质、核酸等生物大分子的空间结构,Kurt Wuithrich等人为此获得2002年诺贝尔化学奖.下列有关13C、15N的叙述中正确的是( )
| A、13C与15N有相同的中子数 |
| B、13C电子排布式为1s22s22p3 |
| C、15N与14N为同位素 |
| D、15N的电子排布式为1s22s22p4 |
考点:原子结构与元素的性质,同位素及其应用
专题:原子组成与结构专题
分析:A.中子数=质量数-质子数;
B.13C原子核外有6个电子,分别位于1s、2s、2p能级上;
C.质子数相同、中子数不同的同一元素互称同位素;
D.15N原子核外有7个电子,分别位于1s、2s、2p能级上.
B.13C原子核外有6个电子,分别位于1s、2s、2p能级上;
C.质子数相同、中子数不同的同一元素互称同位素;
D.15N原子核外有7个电子,分别位于1s、2s、2p能级上.
解答:
解:A.中子数=质量数-质子数,则13C中子数=13-6=7、15N中子数=15-7=8,所以二者中子数不同,故A错误;
B.13C原子核外有6个电子,分别位于1s、2s、2p能级上,13C电子排布式为1s22s22p2,故B错误;
C.15N与14N质子数相同、中子数不同,且属于同一元素的不同原子,互为同位素,故C正确;
D.15N原子核外有7个电子,分别位于1s、2s、2p能级上,15N的电子排布式为1s22s22p3,故D错误;
故选C.
B.13C原子核外有6个电子,分别位于1s、2s、2p能级上,13C电子排布式为1s22s22p2,故B错误;
C.15N与14N质子数相同、中子数不同,且属于同一元素的不同原子,互为同位素,故C正确;
D.15N原子核外有7个电子,分别位于1s、2s、2p能级上,15N的电子排布式为1s22s22p3,故D错误;
故选C.
点评:本题考查了化学用语,涉及原子核外电子排布式的书写、中子数的计算、同位素等知识点,根据基本概念、构造原理等知识点分析即可,属于基础题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
已知土壤胶体粒带负电荷,又有很大的表面积,因而具有选择吸附能力,在土壤里施用含氮量相同的下列氮肥混合物,肥效较差的是( )
| A、(NH4)2SO4 和NH4Cl |
| B、NH4HCO3和NH4Cl |
| C、NH4H2PO4和 NH4HCO3 |
| D、(NH4)2SO4 和NH4NO3 |
鲨鱼是世界上惟一不患癌症的动物,科学研究表明,鲨鱼体内含有一种角鲨烯,具有抗癌性.实验测得角鲨烯分子是链状结构,分子中含有30个碳原子且碳氢质量比为7.2:1,下列说法不正确的是( )
| A、角鲨烯分子式为C30H50 |
| B、1mol角鲨烯最多可与6mol溴单质加成 |
| C、角鲨烯与分子式为C29H48的物质可能属于同系物 |
| D、角鲨烯是高分子化合物 |
有铁的氧化物样品,用140mL 0.5mol/L的盐酸恰好使其完全溶解,所得溶液还能吸收标准状况下氯气56mL,使其中的Fe2+全部转化为Fe3+,该样品可能的化学式是( )
| A、Fe2O3 |
| B、Fe3O4 |
| C、Fe5O7 |
| D、Fe4O5 |
下列化学方程式中,不能用离子方程式Ba2++SO42-═BaSO4 表示的是( )
| A、BaCl2+K2SO4═BaSO4+2 KCl |
| B、Ba(OH)2+K2SO4═BaSO4+2 KOH |
| C、Ba(NO3)2+H2SO4═BaSO4+2 HNO3 |
| D、Ba(OH)2+H2SO4═BaSO4+2 H2O |
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应称取的NaCl的质量是( )
| A、111.2g |
| B、1112.0g |
| C、117.0g |
| D、1170.0g |
有关化学用语正确的是( )
| A、苯的结构简式C6H6 |
| B、乙烯的结构简式CH2CH2 |
C、四氯化碳的电子式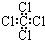 |
| D、乙酸的分子式C2H4O2 |
在一个密闭容器内有X、Y、Z、Q四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
试判断该密闭容器中发生反应属于( )
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 2 | 2 | 48 | 5 |
| 反应后质量/g | 待测 | 24 | 0 | 14 |
| A、化合反应 | B、置换反应 |
| C、复解反应 | D、分解反应 |