题目内容
15.乙烷是一种重要的烷烃,通常用CH3CH3来表示,这种表示法是( )| A. | 电子式 | B. | 结构式 | C. | 结构简式 | D. | 化学式 |
分析 1个乙烷分子中含2个C、6个H,分子式为C2H6,存在C-C、C-H键,结构简式为CH3CH3,以此来解答.
解答 解:A.因碳原子的最外层有4个电子,氢原子最外层1个电子,一个碳原子形成4对共用电子对,一个氢原子形成一对共用电子对,则电子式为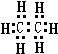 ,故A不选;
,故A不选;
B.乙烷的结构式为 ,故B不选;
,故B不选;
C.由结构式可知,省略单键,乙烷的结构简式为CH3CH3,故C选;
D.乙烷分子式为C2H6,化学式为C2H6,故D不选;
故选C.
点评 本题考查最简式、结构简式、电子式、结构式等,综合考查化学用语,题目难度不大,侧重分析与应用能力的考查,注意乙烷的结构及含有官能团的有机物在书写结构简式时官能团不能省略.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列实验现象描述正确的是( )
| A. | 红磷在空气中燃烧:发出白光,生成大量的白色烟雾 | |
| B. | 碳酸钠溶液与氢氧化钙溶液反应:溶液中产生气泡 | |
| C. | 氢气在空气中燃烧:无色气体燃烧,发出淡蓝色火焰,放热 | |
| D. | 镁条在空气中燃烧:银白色固体燃烧,生成白色固体氧化镁 |
3.下列变化过程中,需要加入氧化剂才能实现的是( )
| A. | Cu→Cu2+ | B. | SO32-→SO2 | C. | Fe2O3→Fe | D. | MnO4-→Mn2+ |
10.在由Na2S、Na2SO3、Na2SO4组成的固体混合物中,已知S的质量分数为32.0%,则氧的质量分数为( )
| A. | 32.0% | B. | 22.0% | C. | 45.0% | D. | 无法计算 |
20.下列仪器:①锥形瓶,②蒸馏烧瓶,③漏斗,④燃烧匙,⑤天平,⑥分液漏斗,⑦胶头滴管.常用于物质分离的是( )
| A. | ①③⑤ | B. | ②④⑦ | C. | ①②⑥ | D. | ②③⑥ |
4.设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
| A. | 1.8 g的NH4+离子中含有的电子数为0.1NA | |
| B. | 1mol Na2O2 固体中含离子总数为4NA | |
| C. | 标准状况下,2.24L CCl4所含的共价键数为O.4NA | |
| D. | 常温常压下,92g NO2和N2O4的混合气体含有的原子数为6NA |
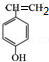
5.R是一种激素类药物,结构简式如图所示.下列说法正确的是( )

| A. | R是芳香烃 | B. | R含2种含氧官能团 | ||
| C. | 1mol R最多与1molH2加成 | D. | R能发生加成、取代和氧化反应 |
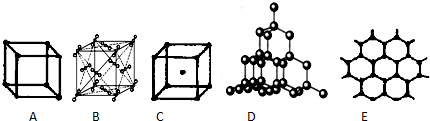
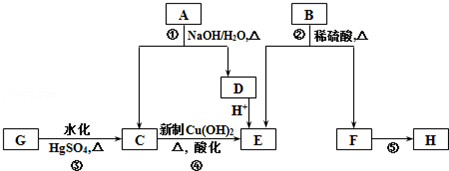
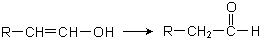
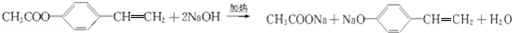 .
.