题目内容
6.锌是一种常用金属,冶炼方法有火法和湿法.I.镓(Ga)是火法冶炼锌过程中的副产品,镓与铝同主族且相邻,化学性质与铝相似,氮化镓(GaN)是制造LED的重要材料,被誉为第三代半导体材料.
(1)Ga在元素周期表中的位置第四周期第IIIA族.
(2)GaN可由Ga和NH3在高温条件下合成,该反应的化学方程式为2Ga+2NH3$\frac{\underline{\;高温\;}}{\;}$2GaN+3H2.
(3)下列有关镓和镓的化合物的说法正确的是ACD(填字母序号).
A.一定条件下,Ga可溶于盐酸和氢氧化钠
B.常温下,Ga可与水剧烈反应放出氢气
C.Ga2O3可由Ga(OH)3受热分解得到
D.一定条件下,Ga2O3可与NaOH反应生成盐
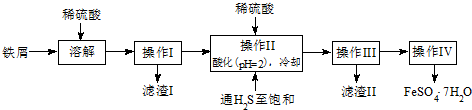
II.甲、乙都是二元固体化合物,将32g甲的粉末加入足量浓硝酸并加热,完全溶解得蓝色溶液,向该溶液中加入足量Ba(NO3)2溶液,过滤、洗涤、干燥得沉淀46.6g;滤液中再滴加NaOH溶液,又出现蓝色沉淀.含乙的矿石自然界中储量较多,称取一定量乙,加入稀盐酸使其全部溶解,溶液分为A、B两等份,向A中加入足量氢氧化钠溶液,过滤、洗涤、灼烧得红棕色固体28g,经分析乙与红棕色固体的组成元素相同,向B中加入8.0g铜粉充分反应后过滤、洗涤、干燥得剩余固体1.6g.
(1)32g甲在足量浓硝酸中反应转移的电子数为2NA;甲在足量氧气中充分灼烧的化学方程式为Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2
(2)乙的化学式Fe7O9;稀硫酸溶解乙的化学方程式为9H2SO4+Fe7O9=3FeSO4+2Fe2(SO4)3+9H2O
(3)将甲在足量氧气中充分灼烧的气体产物通入一定量A溶液中,该反应的离子方程式为SO2+2Fe3++2H2O=2Fe2++SO42-+4H+,设计实验证明此步反应后的溶液中金属元素的化合价取反应后的溶液两份于试管中,向一份中加入酸化的KMnO4溶液,若褪色,则含有+2价铁,向另一份中加入KSCN溶液,若出现血红色溶液,则含有+3价铁.
分析 I.(1)Ga的原子序数为31,位于第四周期第ⅢA族;
(2)Ga和NH3在高温条件下反应生成GaN和氢气;
(3)镓位于第ⅢA族,位于金属与非金属交界处,与Al具有相似性质,金属性比Al强,以此分析其单质和化合物的性质;
II.将32g甲的粉末加入足量浓硝酸并加热,完全溶解得蓝色溶液,向该溶液中加入足量Ba(NO3)2溶液,过滤、洗涤、干燥得沉淀46.6g,该沉淀为硫酸钡,其物质的量为:$\frac{46.6g}{233g/mol}$=0.2mol,根据质量守恒可知甲中含有0.2molS原子;滤液中再滴加NaOH溶液,又出现蓝色沉淀,该蓝色沉淀为氢氧化铜,说明甲中含有Cu离子,32g甲中含有铜元素的物质的量为:$\frac{32g-32g/mol×0.2mol}{64g/mol}$=0.4mol,则甲的化学式为:Cu2S;
含乙的矿石自然界中储量较多,称取一定量乙,加入稀盐酸使其全部溶解,溶液分为A、B两等份,向A中加入足量氢氧化钠溶液,过滤、洗涤、灼烧得红棕色固体28g,该红棕色固体为Fe2O3,氧化铁含有铁元素的物质的量为额:$\frac{28g}{160g/mol}$×2=0.35mol,可能为铁离子和亚铁离子的混合物;经分析乙与红棕色固体的组成元素相同,则乙中含有Fe、O元素;向B中加入8.0g铜粉充分反应后过滤、洗涤、干燥得剩余固体1.6g,反应消耗铜的物质的量为:$\frac{8.0g-1.6g}{64g/mol}$=0.1mol,根据反应2Fe3++Cu═2Fe2++Cu2+可知,0.1mol铜完全反应消耗0.2molFe3+;所以乙与盐酸反应生成的为0.2molFe3+、0.15molFe2+,铁的平均化合价为:$\frac{0.2mol×3+0.15mol×2}{0.35mol}$=$\frac{18}{7}$,则乙的化学式为:Fe7O9,据此分析解答.
解答 解:(1)Ga的原子序数为31,位于第四周期第ⅢA族,故答案为:第四周期第ⅢA族;
Ga和NH3在高温条件下反应生成GaN和氢气,反应为2Ga+2NH3$\frac{\underline{\;高温\;}}{\;}$2GaN+3H2,故答案为:2Ga+2NH3$\frac{\underline{\;高温\;}}{\;}$2GaN+3H2;
(3)镓位于第ⅢA族,位于金属与非金属交界处,与Al具有相似性质,则:
A.Al与盐酸、NaOH均反应,则一定条件下,Ga可溶于盐酸和氢氧化钠,故A正确;
B.Al与水常温不反应,则常温下,Ga不能与水剧烈反应放出氢气,故B错误;
C.氧化铝可由氢氧化铝分解生成,则Ga2O3可由Ga(OH)3受热分解得到,故C正确;
D.氧化铝与NaOH反应生成盐,则一定条件下,Ga2O3可与NaOH反应生成盐,故D正确;
故答案为:ACD
II.将32g甲的粉末加入足量浓硝酸并加热,完全溶解得蓝色溶液,向该溶液中加入足量Ba(NO3)2溶液,过滤、洗涤、干燥得沉淀46.6g,该沉淀为硫酸钡,其物质的量为:$\frac{46.6g}{233g/mol}$=0.2mol,根据质量守恒可知甲中含有0.2molS原子;滤液中再滴加NaOH溶液,又出现蓝色沉淀,该蓝色沉淀为氢氧化铜,说明甲中含有Cu离子,32g甲中含有铜元素的物质的量为:$\frac{32g-32g/mol×0.2mol}{64g/mol}$=0.4mol,则甲的化学式为:Cu2S;
含乙的矿石自然界中储量较多,称取一定量乙,加入稀盐酸使其全部溶解,溶液分为A、B两等份,向A中加入足量氢氧化钠溶液,过滤、洗涤、灼烧得红棕色固体28g,该红棕色固体为Fe2O3,氧化铁含有铁元素的物质的量为额:$\frac{28g}{160g/mol}$×2=0.35mol,可能为铁离子和亚铁离子的混合物;经分析乙与红棕色固体的组成元素相同,则乙中含有Fe、O元素;向B中加入8.0g铜粉充分反应后过滤、洗涤、干燥得剩余固体1.6g,反应消耗铜的物质的量为:$\frac{8.0g-1.6g}{64g/mol}$=0.1mol,根据反应2Fe3++Cu═2Fe2++Cu2+可知,0.1mol铜完全反应消耗0.2molFe3+;所以乙与盐酸反应生成的为0.2molFe3+、0.15molFe2+,铁的平均化合价为:$\frac{0.2mol×3+0.15mol×2}{0.35mol}$=$\frac{18}{7}$,则乙的化学式为:Fe7O9,
(1)甲为Cu2S,32gCu2S的物质的量为:$\frac{32g}{160g/mol}$=0.2mol,浓硝酸足量,Cu元素从+1转化成+2价、硫元素从-2转化成+6价,则反应中失去电子总物质的量为:0.2mol×2×(2-1)+0.2mol×[6-(-2)]=2mol,反应转移电子总数为2NA;甲在足量空气中灼烧生成氧化铜、二氧化硫气体,反应的化学方程式为:Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2,
故答案为:2NA;Cu2S+2O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+SO2;
(2)根据分析可知,乙的化学式为:Fe7O9;稀硫酸与乙反应的化学方程式为:9H2SO4+Fe7O9=3FeSO4+2Fe2(SO4)3+9H2O,
故答案为:Fe7O9;9H2SO4+Fe7O9=3FeSO4+2Fe2(SO4)3+9H2O;
(3)甲在足量氧气中充分灼烧的气体产物是二氧化硫,A中含有铁离子,二氧化硫和铁离子发生氧化还原反应生成亚铁离子和硫酸根离子,离子方程式为SO2+2Fe3++2H2O=2Fe2++SO42-+4H+,向溶液中加入强氧化剂将亚铁离子氧化为铁离子,然后用KSCN检验铁离子,所以其检验方法为:取反应后的溶液两份于试管中,向一份中加入酸化的KMnO4溶液,若褪色,则含有+2价铁,向另一份中加入KSCN溶液,若出现血红色溶液,则含有+3价铁,
故答案为:SO2+2Fe3++2H2O=2Fe2++SO42-+4H+;取反应后的溶液两份于试管中,向一份中加入酸化的KMnO4溶液,若褪色,则含有+2价铁,向另一份中加入KSCN溶液,若出现血红色溶液,则含有+3价铁.
点评 本题考查无机物推断及同一主族元素周期律,为高频考点,侧重考查学生推断及知识综合运用能力,明确常见元素化合物性质、元素周期律内涵是解本题关键,难点是II的物质推断,题目难度中等.

| A. | H2O2的电子式: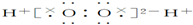 | |
| B. | NH4I的电子式: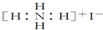 | |
| C. | 原子核内有10个中子的氧原子:1810O | |
| D. | CO2分子的结构式:O═C═O |
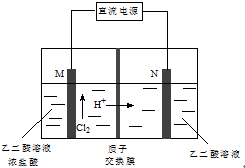 乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法正确的是( )
乙醛酸(HOOC-CHO)是有机合成的重要中间体.工业上用“双极室成对电解法”生产乙醛酸,原理如图所示.该装置中阴、阳两极为惰性电极,两极室均可产生乙醛酸,其中乙二醛与M电极的产物反应生成乙醛酸.下列说法正确的是( )| A. | M极与直流电源的负极相连 | |
| B. | 若有2 molH+通过质子交换膜并完全参与反应,则该装置中生成的乙醛酸为1 mol | |
| C. | N电极上的电极反应式:HOOC-COOH-2e-+2H+=HOOC-CHO+H2O | |
| D. | 乙二醛与M电极的产物反应生成乙醛酸的化学方程式:Cl2+OHC-CHO+H2O=HOOC-CHO+2HCl |
| A. | Na2CO3溶液 | B. | BaCl2溶液 | C. | Ba(OH)2溶液 | D. | Fe(OH)3胶体 |
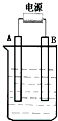 在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题:
在如图用石墨作电极的电解池中,放入500mL含一种溶质的某蓝色溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成;当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6g.请回答下列问题: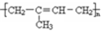 )为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.
)为主要成分的天然高分子化合物.天然橡胶有两种,一种是巴西三叶橡胶树产出的橡胶,通常就称为天然橡胶;另一种是杜仲树产出的橡胶,它是我国特产,在湖北等地都有大面积种植,被称为杜仲胶.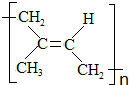 .
.