题目内容
12.下列各组物质中,所含分子数相同的是( )| A. | 10gH2和10gO2 | B. | 11.2LN2(标准状况下)和11gCO | ||
| C. | 9gH2O和0.5mol Br2 | D. | 224mlH2(标准状况下)和0.1mol N2 |
分析 所含分子数相等,说明两种物质的物质的量相等,根据n=$\frac{m}{M}$=$\frac{V}{Vm}$计算其物质的量来判断即可.
解答 解:A.氢气与氧气摩尔质量不同,所以依据n=$\frac{m}{M}$可知,质量相同的氢气和氧气,物质的量不同,分子数不同,故A错误;
B.氮气的物质的量为$\frac{11.2L}{22.4L/mol}$=0.5mol,11gCO的物质的量为$\frac{11g}{30g/mol}$≠0.5mol,二者物质的量不同,分子数不同,故B错误;
C.9gH2O物质的量为$\frac{9g}{18g/mol}$=0.5mol,与溴单质的物质的量相等,所以分子数相同,故C正确;
D.224mL氢气物质的量为$\frac{0.224L}{22.4L/mol}$=0.01mol,与氮气的物质的量不同,所以分子数不同,故D错误;
故选:C.
点评 本题考查物质的量的计算,侧重考查分析计算能力,明确物质的量公式中各个物理量的关系即可解答,注意气体摩尔体积适用范围及适用条件,题目难度不大.

练习册系列答案
相关题目
2.某化妆品的组分Z具有美白功效,原料从杨树中提取,现可用如图反应制备,下列叙述错误的是( )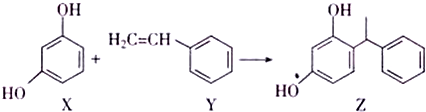

| A. | X、Y和Z均能使溴水褪色,且原理相同 | |
| B. | X和Z均能与Na2CO3溶液反应放出CO2 | |
| C. | Z中含手性碳原子 | |
| D. | Y可作加聚反应的单体,X可作缩聚反应的单体 |
3.将20gM物质、5gN物质、9gP物质混合加热发生化学变化,经充分反应后的混合物中含有5gM物质、20gP物质还含有一种新物质Q,若M、N、P、Q的相对分子质量分别为30、20、44、18,它们之间发生反应的化学方程式是( )
| A. | M+N=P+Q | B. | M+2N=2P+Q | C. | 2M+N=2P+Q | D. | 2M+N=P+2Q |
20.铁粉和水蒸气反应的装置如图所示,有关该反应的说法正确的是( )


| A. | 该反应属于复分解反应 | |
| B. | 网罩的作用是集中火焰,提高温度 | |
| C. | 湿棉花的作用是给试管降温,防止炸裂 | |
| D. | 反应中水既不是氧化剂,也不是还原剂 |
17.下面关于硅的叙述中,正确的是( )
| A. | 粗硅制备单晶硅不涉及氧化还原反应 | |
| B. | 硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 | |
| C. | 硅的化学性质不活泼,在自然界中可以以游离态存在 | |
| D. | 硅在电子工业中,是重要的半导体材料 |
4.“嫦娥奔月”是一个充满浪漫主义的中国神话故事.2007年10月24日我国“嫦娥一号”探月卫星由长三甲火箭送入预定的轨道.长三甲火箭第三级推进剂采用低温液氧/液氢.已知在298K时,2g氢气与氧气完全反应生成液态水放热285.8kJ,则此反应的热化学方程式为( )
| A. | 2H2(g)+O2(g)═2H2O(l)△H=-285.8KJ•mol-1 | |
| B. | 2H2(g)+O2(g)═2H2O(l)△H=+285.8KJ•mol-1 | |
| C. | 2H2(g)+O2(g)═2H2O(l)△H=-571.6KJ•mol-1 | |
| D. | 2H2(g)+O2(g)═2H2O(l)△H=+571.6KJ•mol-1 |