题目内容
17.下列措施能促进CH3COONa水解的是( )| A. | 加入少量KOH固体 | B. | 加入少量NaCl固体 | ||
| C. | 加入少量K2S固体 | D. | 加热 |
分析 醋酸钠溶液中存在醋酸根离子水解平衡:CH3COO-+H2O?CH3COOH+OH-,若促进醋酸钠的水解,需要使该水解平衡向着正向移动,如加水稀释、升高温度等,据此进行解答.
解答 解:醋酸钠溶液中存在醋酸根离子水解平衡:CH3COO-+H2O?CH3COOH+OH-,
A.加入氢氧化钾固体后,氢氧根离子浓度增大,抑制了醋酸根离子的水解,故A错误;
B.加入少量NaCl固体,氯离子和钠离子不影响该平衡,故B错误;
C.加入少量K2S固体,硫离子水解使溶液呈碱性,溶液中氢氧根离子浓度增大,抑制了醋酸根离子的水解,故C错误;
D.盐的水解为吸热反应,加热后可以常见醋酸钠的水解,故D正确;
故选D.
点评 本题考查了盐的水解原理及其影响,题目难度不大,明确影响盐的水解平衡的因素为解答关键,注意盐的水解为吸热反应,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
7.下列离子方程式中正确的是( )
| A. | 铜与热的稀硫酸:Cu+2H+═Cu2++H2↑ | |
| B. | 在碳酸氢铵稀溶液中加入足量的氢氧化钠稀溶液:NH4++OH-═NH3•H2O | |
| C. | AlCl3溶液滴加过量的氨水:3NH3•H2O+Al3+═Al(OH)3↓+3NH4+ | |
| D. | 氯化亚铁溶液中通入氯气:Fe2++Cl2═Fe3++2Cl- |
8.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在标准状况下,22.4L SO3的分子数约为NA个 | |
| B. | 58.5g NaCl溶于1 L水中,所得溶液中溶质的物质的量浓度为1 mol/L | |
| C. | 常温、常压下,48g臭氧含有的氧原子数为3NA | |
| D. | 5.6g Fe与足量的盐酸反应失去的电子数为0.3NA |
5.如图所示的实验操作中,正确的是( )
| A. |  检查容器瓶是否漏水 | B. | 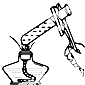 给溶液加热 | ||
| C. | 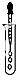 滴加液体 | D. | 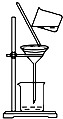 过滤 |
2.下列实验操作或事故处理正确的是( )
| A. | 分液时,打开分液漏斗旋转活塞,先放出下层液体,再放出上层液体 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶的支管口处 | |
| C. | 皮肤不慎沾上NaOH溶液,立即用盐酸冲洗 | |
| D. | 过滤时,为了加快速度,用玻璃棒搅拌悬浊液 |
9.下列实验方法错误的是( )
| A. | 除去氯化钾中混有的KI:溶于水通入过量氯气,蒸发结晶 | |
| B. | 除去Na2CO3固体中混有的NaHCO3:加热至恒重 | |
| C. | 除去食盐中的泥沙:溶于水,过滤,滤液蒸发结晶 | |
| D. | 从溴水中提取溴单质:加入酒精萃取 |
6.下列化学用语书写正确的是( )
| A. | 乙烯的结构简式 CH2CH2 | |
| B. | 氯离子的结构示意图: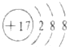 | |
| C. | H2O的电子式: | |
| D. | 碳酸钾的电离方程式 K2SO4=K2++SO42- |
7.14g铜银合金与足嫩的某浓度的硝酸反应,将放出的气体与1.12L(标准状况下)氧气混合,通入水中恰好全部被吸收,则合金中铜的质量为( )
| A. | 9.6g | B. | 6.4g | C. | 3.2g | D. | 1.6g |
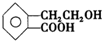 ,它可通过不同化学反应分别制得B、C、D和E四种物质.
,它可通过不同化学反应分别制得B、C、D和E四种物质.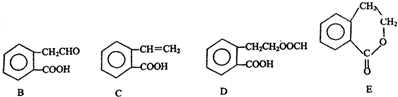
 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2 +2H2O.
+2H2O.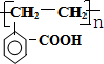 .
.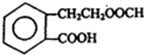 +2NaOH$\stackrel{△}{→}$HCOONa+
+2NaOH$\stackrel{△}{→}$HCOONa+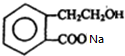 +2H2O.
+2H2O.