题目内容
5.如图所示的实验操作中,正确的是( )| A. |  检查容器瓶是否漏水 | B. | 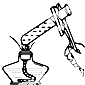 给溶液加热 | ||
| C. | 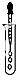 滴加液体 | D. | 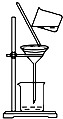 过滤 |
分析 A.容量瓶检漏时要倒置容量瓶;
B.给试管内液体加热时,用酒精灯外焰加热;
C.向试管中滴加液体时,胶头滴管不能伸入试管内;
D.过滤时,漏掉低端尖嘴部分要紧靠烧杯内壁.
解答 解:A.容量瓶检漏时要倒置容量瓶,根据是否流出液体检验容量瓶,故A正确;
B.给试管内液体加热时,用酒精灯外焰加热,酒精灯外焰温度较高,故B错误;
C.向试管中滴加液体时,胶头滴管不能伸入试管内,否则易污染胶头滴管,故C错误;
D.过滤时,漏掉低端尖嘴部分要紧靠烧杯内壁,否则会溅出液体,故D错误;
故选A.
点评 本题考查化学实验方案评价,为高频考点,涉及仪器的使用、基本实验操作等知识点,明确仪器用途、基本操作规范性是解本题关键,易错选项是C,只有制取氢氧化亚铁沉淀时胶头滴管能伸入试管中.

练习册系列答案
相关题目
15.元素周期表是学习化学的重要工具,它包含了许多的信息和规律.下表是元素周期表的一部分,请从下表①~⑧十种元素中选择适当的元素回答下列问题:
(1)原子半径最大的元素在周期表中的位置是第三周期第IA族.
(2)③⑦⑧三元素与①形成的气态氢化物稳定性最差的是H2S(填化学式).
(3)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是Al(OH)3,(填写化学式),该氢氧化物呈两性的原因:H++AlO2-+H2O?Al(OH)3?Al3++3OH-.(用电离方程式表示)
(4)元素⑥和Fe比较,金属性较强的元素是Al(填元素符号)用一个化学反应可以证明元素⑥和Fe的金属性的强弱,写出该反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
| 族 周期 | I A | II A | III A | IV A | VA | VI A | VII A |
| 1 | ① | ||||||
| 2 | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | |||
(2)③⑦⑧三元素与①形成的气态氢化物稳定性最差的是H2S(填化学式).
(3)在这些元素的最高价氧化物对应水化物中,呈两性的氢氧化物是Al(OH)3,(填写化学式),该氢氧化物呈两性的原因:H++AlO2-+H2O?Al(OH)3?Al3++3OH-.(用电离方程式表示)
(4)元素⑥和Fe比较,金属性较强的元素是Al(填元素符号)用一个化学反应可以证明元素⑥和Fe的金属性的强弱,写出该反应的化学方程式:2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.
16.下列物质的提纯方法可能属于化学变化的是( )
| A. | 萃取 | B. | 除杂 | C. | 分液 | D. | 过滤 |
13.下列与实验相关的叙述正确的是( )
| A. | 金属钠着火时,用细沙覆盖灭火,镁着火用泡沫灭火器 | |
| B. | 用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准液润洗,则待测结果会偏低 | |
| C. | 测定一包白色粉末的质量,将药品放在右盘,砝码放在左盘 | |
| D. | 除去乙醇中的乙酸可先加入碳酸钠溶液然后蒸馏 |
20.某同学设计如下元素周期表,下列说法正确的是( )
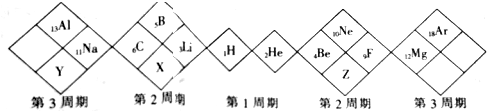

| A. | X元素最高价氧化物对应的水化物为弱酸 | |
| B. | Y元素最外层电子数是最内层电子数的2倍 | |
| C. | 原子半径:Y>X>Z | |
| D. | X、Y、Z的气态氢化物中最稳定的是X的氢化物 |
10.1体积某有机物蒸气与4体积氧气恰好反应,生成二氧化碳和水,反应后混合气体的密度比反应前的密度减小了$\frac{1}{6}$(气体体积都在150℃、1.01×105Pa时测定).此有机物的分子式是( )
| A. | C3H8 | B. | C3H8O2 | C. | C2H6O | D. | C3H6O |
17.下列措施能促进CH3COONa水解的是( )
| A. | 加入少量KOH固体 | B. | 加入少量NaCl固体 | ||
| C. | 加入少量K2S固体 | D. | 加热 |
14.已知某元素+2价阳离子的电子排布式为1s22s22p63s23p6,该元素在周期表中属于( )
| A. | ⅤB族 | B. | ⅡB族 | C. | Ⅷ族 | D. | ⅡA族 |