题目内容
3.下列各组晶体中化学键类型和晶体类型均相同的是( )| A. | 二氧化硅和二氧化碳 | B. | 金刚石和石墨 | ||
| C. | 氯化钠和过氧化钠 | D. | 溴和白磷 |
分析 A.二氧化硅是原子晶体,二氧化碳是分子晶体,二氧化硅存在共价键,二氧化碳分子内为共价键,分子间为范德华力;
B.金刚石是原子晶体,石墨属于混合晶体,金刚石存在共价键,石墨层内为共价键,层间为范德华力;
C.氯化钠是离子晶体,过氧化钠为离子晶体,氯化钠存在离子键,过氧化钠既存在离子键,也存在共价键;
D.溴是分子晶体,白磷是分子晶体,均存在共价键.
解答 解:A.二氧化硅是原子晶体,存在共价键,二氧化碳是分子晶体,分子内为共价键,分子间为范德华力,二者晶体类型和化学键类型不同,故A不选;
B.金刚石是原子晶体,存在共价键,石墨为层状晶体,层内是共价键,层间是范德华力,属混合晶体,二者化学键类型和晶体类型不同,故B不选;
C.氯化钠是离子晶体,存在离子键,过氧化钠为离子晶体,但既存在离子键,也存在共价键,二者化学键类型不相同,故C不选;
D.溴是分子晶体,白磷是分子晶体,均存在共价键.二者化学键类型和晶体类型均相同,故D选;
故选D.
点评 本题考查化学键类型和晶体类型的判断,分清原子晶体,分子晶体,离子晶体等常见晶体的化学键是解答的关键.本题难度不大,是基础题.

练习册系列答案
相关题目
9.下列方程式书写正确的是( )
| A. | 碳酸钠的水解反应:CO32-+H3O+?HCO3-+H2O | |
| B. | 氢氧化铁胶体的制备:Fe3++3OH-═Fe(OH)3(胶体) | |
| C. | 偏铝酸钠中滴加碳酸氢钠溶液:AlO2-+HCO3-+H2O═Al(OH)3↓+CO32- | |
| D. | 碱性氢氧燃料电池的正极反应式:4OH--4e-═2H2O+O2↑ |
14.下列关于碱金属及其化合物的说法不正确的是( )
| A. | 从锂到铯与水反应越来越剧烈 | B. | 液态钠可用作核反应堆的传热介质 | ||
| C. | Li在氧气中燃烧生成Li2O2 | D. | 氢氧化铯的碱性强于氢氧化钠 |
11.下列关于电解质溶液的叙述正确的是( )
| A. | 将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 | |
| B. | 常温下,饱和氯水中c(H+)-c(OH-)═c(Cl-)+C(ClO-) | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH小 |
18.运用下列装置和操作能达到实验目的和要求的是( )

| A. | 用①分离氯化铵和单质碘 | |
| B. | 用②除去淀粉溶液中的氯化钠 | |
| C. | 用③加热胆矾(CuSO4•5H2O)制取无水硫酸铜 | |
| D. | 用④装置收集NO或CO |
8.已知碳碳单键可以绕键轴自由旋转,结构简式为如图所示的有机物,下列说法中正确的是( )
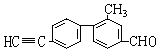

| A. | 分子中处于同一直线上的碳原子最多有7个 | |
| B. | 分子中至少有16个碳原子处于同一平面上 | |
| C. | 该有机物可发生加成反应和消去反应 | |
| D. | 该有机物分子式C16H10O |
15.下列晶体中,它们的熔点由高到低的顺序排列正确的是( )
①金刚石 ②氯化钠 ③干冰 ④汞.
①金刚石 ②氯化钠 ③干冰 ④汞.
| A. | ④②③① | B. | ①②④③ | C. | ④②①③ | D. | ③④②① |
 )有如下转化关系:
)有如下转化关系:
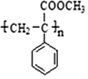 .
. .
. .
.