题目内容
在25℃时,向100mL含氯化氢14.6g的盐酸中放入5.6g纯铁粉(不考虑反应前后溶液体积的变化),反应开始到2min末收集到H2 1.12L(标准状况下),在此之后又经过4min,铁粉完全溶解.则:
(1)在前2min内用FeCl2的浓度变化表示的平均反应速率是多少?
(2)在后4min内用HCl的浓度变化表示的平均反应速率是多少?
(3)前2min与后4min相比,反应速率哪个较快?
(1)在前2min内用FeCl2的浓度变化表示的平均反应速率是多少?
(2)在后4min内用HCl的浓度变化表示的平均反应速率是多少?
(3)前2min与后4min相比,反应速率哪个较快?
考点:反应速率的定量表示方法
专题:化学反应速率专题
分析:根据Fe+2HCl=FeCl2+H2↑,根据2min末收集到H2 1.12L(标准状况下),6min时反应了5.6g铁粉计算生成n(FeCl2),结合v=
=
变形进行计算、比较.
| △c |
| △t |
| △n |
| V?△t |
解答:
解:化学方程式为:Fe+2HCl=FeCl2+H2↑
2 min末时:n(FeCl2)=n(H2)=
=0.05 mol,
c(FeCl2)=
=0.5 mol?L-1
6 min末时:n(FeCl2)=n(Fe)=
=0.1 mol,c(FeCl2)=
=1.0 mol?L-1
(1)前2min内:v(FeCl2)=
=
=0.25 mol?L-1?min-1
(2)后4 min内:v(FeCl2)=
=
=0.125 mol?L-1?min-1
v(HCl)=2v(FeCl2)=0.125 mol?L-1?min-1×2=0.25 mol?L-1?min-1
(3)选用v(FeCl2)比较,因为0.25 mol?L-1?min-1>0.125mol?L-1?min-1,所以前2 min内反应速率快.
答:(1)v(FeCl2)=0.25mol?L-1?min-1;(2)v(HCl)=0.25 mol?L-1?min-1;(3)前2 min内反应速率快.
2 min末时:n(FeCl2)=n(H2)=
| 1.12L |
| 22.4L/mol |
c(FeCl2)=
| 0.05mol |
| 0.1L |
6 min末时:n(FeCl2)=n(Fe)=
| 5.6g |
| 56g/mol |
| 0.1mol |
| 0.1L |
(1)前2min内:v(FeCl2)=
| △c(FeCl2) |
| △t |
| 0.5mol/L-0 |
| 2min |
(2)后4 min内:v(FeCl2)=
| △c(FeCl2) |
| △t |
| 1.0mol/L-0.5mol/L |
| 4min |
v(HCl)=2v(FeCl2)=0.125 mol?L-1?min-1×2=0.25 mol?L-1?min-1
(3)选用v(FeCl2)比较,因为0.25 mol?L-1?min-1>0.125mol?L-1?min-1,所以前2 min内反应速率快.
答:(1)v(FeCl2)=0.25mol?L-1?min-1;(2)v(HCl)=0.25 mol?L-1?min-1;(3)前2 min内反应速率快.
点评:本题考查了化学反应速率的计算,综合性较强,通过化学方程式计算出2min和6min时生成n(FeCl2)是解题的关键,题目难度一般.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案
相关题目
醇类化合物在香料中占有重要的地位,下面所列的是一些天然的或合成的醇类香料:
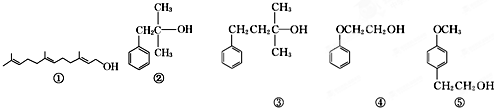
下列说法中正确的是( )

下列说法中正确的是( )
| A、可用酸性KMnO4溶液检验①中是否含有碳碳双键 |
| B、②和③互为同系物,均能催化氧化生成醛 |
| C、④和⑤互为同系物,可用核磁共振氢谱检验 |
| D、等物质的量的上述5种有机物与足量的金属钠反应,消耗钠的量相同 |
我国具有悠久的酿酒历史,某白酒标签上标有“53°”字样,它表示( )
| A、该酒是在53℃条件下酿制的 |
| B、该酒的着火点为53℃ |
| C、100 mL该酒中含有53 mL酒精 |
| D、100g该酒中含有53g酒精 |