��Ŀ����
����Ŀ����A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʿ����ᷴӦ�� 1mol E���������������ã��ڱ�״�����ܲ���33.6LH2��E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ���ش��������⣺

��1��AԪ�ص�����Ϊ____________��D���ӵĽṹʾ��ͼΪ_____________��
��2��C�����ڱ��е�λ��Ϊ______________________��
��3��Ԫ��C��Ԫ��D��ȣ��ǽ����Խ�ǿ����__________����Ԫ�ط��ű�ʾ�������б�������֤����һ��ʵ����________��������ĸ��ţ�
a��������C�ĵ��ʺ�D�ĵ���״̬��ͬ
b��D����̬�⻯���C����̬�⻯���ȶ�
c��һ��������C��D�ĵ��ʶ���������������Һ��Ӧ
d��D������������ˮ��������Ա�C������������ˮ���������ǿ
e��D�ĵ����ܺ�C��������Һ��Ӧ����C�ĵ���
��4��Ԫ��A��һ���⻯�ﺬ�зǼ��Լ���A�������⻯��ĵ���ʽ��____________��
��5��A��C��D��EԪ���γɵļ����Ӱ뾶�Ĵ�С˳����________���������ӷ��ű�ʾ��
��6��E������������Ӧ��ˮ���������������Һ��Ӧ�Ļ�ѧ����ʽ��________________��
���𰸡��� 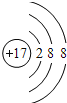 �������ڢ�A�� Cl bde
�������ڢ�A�� Cl bde ![]() S2- > Cl- > O2- > Al3+ Al(OH)3 + NaOH = NaAlO2 + 2H2O
S2- > Cl- > O2- > Al3+ Al(OH)3 + NaOH = NaAlO2 + 2H2O
��������
A��B��C��D��E���ֶ�����Ԫ�أ�����Ԫ�����ڱ�֪��������Ԫ�ش��ڵڶ��������ڣ���C��ԭ��������X����A��B��D��ԭ�������ֱ���(X-8)��(X-1)��(X+1)�����ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ���(X-8)+(X-1)+X+(X+1)=56����X=16������C��SԪ�أ�A��OԪ�أ�B��PԪ�أ�D��ClԪ�أ�E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2����һ��Eԭ��ʧȥ3���������������ӣ�E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ����E��AlԪ�أ��Դ˽����⡣
A��B��C��D��E���ֶ�����Ԫ�أ�����Ԫ�����ڱ�֪��������Ԫ�ش��ڵڶ��������ڣ���C��ԭ��������X����A��B��D��ԭ�������ֱ���(X-8)��(X-1)��(X+1)�����ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ���(X-8)+(X-1)+X+(X+1)=56����X=16������C��SԪ�أ�A��OԪ�أ�B��PԪ�أ�D��ClԪ�أ�E�ĵ��ʿ����ᷴӦ��1molE���������������ã��ڱ�״�����ܲ���33.6LH2����һ��Eԭ��ʧȥ3���������������ӣ�E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ����E��AlԪ�أ�
(1)�ɷ�����֪AΪO��Ԫ�ص�����Ϊ����DΪClԪ�أ�Cl-���ӵĽṹʾ��ͼΪ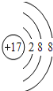 ��
��
(2)CΪ��Ԫ�أ��˵����Ϊ16��ԭ�ӽṹʾ��ͼΪ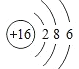 �����������ڱ��е�λ��Ϊ�������ڢ�A�壻
�����������ڱ��е�λ��Ϊ�������ڢ�A�壻
(3)ͬ��������Ԫ�غ˵������Ԫ�صķǽ�����ǿ����ClԪ�طǽ����Ա�SԪ��ǿ��
a������״̬�����������ʣ����ܱȽ�Ԫ�طǽ����ԣ���a����
b���⻯���ȶ�����Ԫ�طǽ�����һ�£��Ȼ���������ȶ���˵���ȵķǽ����Ը�ǿ����b��ȷ��
c��һ��������Cl2��S����������������Һ��Ӧ��֤��S��Cl2�����������ԣ����л�ԭ�ԣ��������ж������ȵķǽ�����ǿ������c����
d��Ԫ�صķǽ�����Խǿ�����������ˮ���������Խǿ����Cl������������ˮ��������Ա�S������������ˮ���������ǿ��˵��Cl�ķǽ����Ա�Sǿ����d��ȷ��
e��Cl2�ܺ�Na2S��Һ��Ӧ����S���ʣ�˵��Cl�ķǽ����Ա�Sǿ����e��ȷ��
�ʴ�Ϊbde��
(4)Ԫ��AΪ������HԪ����ɵĻ�����H2O2�к��зǼ��Լ���H2O2�ĵ���ʽ��![]() ��
��
(5)O2-��Al3+��S2-��Cl-�����ӽṹ��ͬ���˵���������Ӱ뾶С����S2-��Cl-�����ӽṹ��O2-��Al3+��һ�����Ӳ㣬�����������ӵ����Ӱ뾶�ɴ�С��˳��ΪS2-��Cl-��O2- �� Al3+��
(6)Al(OH)3������������Һ��Ӧ����ƫ�����ƺ�ˮ����Ӧ�Ļ�ѧ����ʽ��Al(OH)3 + NaOH = NaAlO2 + 2H2O��

 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
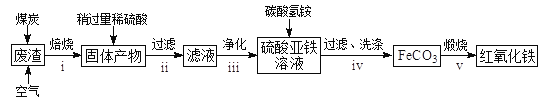
Сѧ��10����Ӧ����ϵ�д�����Ŀ���̷�(FeSO4��7H2O)�ڹ�ҵ�Ͽ������������Ρ��������켰����ȡ���������������м(����������������������)Ϊԭ�����������̷���һ�ַ�����

25�� | pHֵ |
����H2S��Һ | 3.9 |
SnS������ȫ | 1.6 |
FeS��ʼ���� | 3.0 |
FeS��ʼ���� | 5.5 |
��1�������Ƶõ��̷��������Ƿ���Fe3�������ѡ�õ��Լ�Ϊ________��
A��KSCN��Һ B��NaOH��Һ C��KMnO4��Һ D��������Һ
��2���������У�ͨ�����������͵�Ŀ����______________________________________������Һ���������ữ��pH��2��Ŀ����__________________________________��
��3����������˳������Ϊ_________________����ȴ�ᾧ��____________________��
��4���������õ����̷�������������ˮϴ�ӣ���Ŀ���ǣ��ٳ�ȥ������渽�ŵ���������ʣ���_________________________________________________________��
��5���ⶨ�̷���Ʒ��Fe2�������ķ����ǣ�a.��ȡ2.850 g�̷���Ʒ���ܽ⣬��250 mL����ƿ�ж��ݣ�b.��ȡ25.00 mL������Һ����ƿ�У�c.�������ữ��0.010 00 mol��L��1 KMnO4��Һ�ζ����յ㣬����KMnO4��Һ�����ƽ��ֵΪ20.00 mL��
�ٵζ�ʱʢ��KMnO4��Һ������Ϊ________________________(����������)��
�ڼ���������Ʒ��FeSO4��7H2O����������Ϊ____________________��